心脑血管疾病长期位居全球疾病负担与死亡原因的首位,其中心脏与脑部的血管病变曾长期被作为独立的病理体系开展研究;近年来的研究逐步揭示,醛固酮失调作为肾素-血管紧张素-醛固酮系统功能紊乱的核心标志,是串联两类器官损伤、推动共病进展的关键调控轴,引发了学者的关注。在第一届长三角心血管代谢管理多学科学术会议上,复旦大学附属华山医院心内科包丽雯副主任医师以“神经心脏病学视角下探讨醛固酮失调”为题,从神经心脏病学的角度,探讨了醛固酮对心脑血管疾病的影响。

一、临床迷思:
心悸、脑出血与难治性高血压的共同“元凶”
临床中,部分高血压患者的病情格外棘手——不仅血压难以控制,还常伴随看似毫无关联的严重并发症。以下2例代表性病例,揭示了阵发性房颤、脑脑血管意外与原发性醛固酮增多症背后可能潜藏的共同病理生理基础。
病例1:
反复心悸、血压飙升的七旬老人
病例概述:74岁男性,高血压病史30余年,口服ARB+CCB方案,平素血压控制尚可,后因多次突发快速心室率心房颤动(1年已反复发作3次)伴血压升高(178/98 mmHg)急诊就诊。
此次急诊生化学关键线索:血钾偏低(3.1 mmol/L)。门诊筛查继发性高血压病因:醛固酮196.3 pg/ml,醛固酮与肾素活性比值(ARR)78.5。入院生理盐水负荷试验阳性(试验后,血浆醛固酮107.8 pg/ml)。完善肾上腺增强CT提示双侧肾上腺增生。
诊断:原发性醛固酮增多症(PA)。
病例2:
难治性高血压合并脑出血史的患者
病例概述:62岁男性,高血压病史30余年,长期口服血管紧张素Ⅱ受体拮抗剂(ARB)、钙通道阻滞剂(CCB)及噻嗪类利尿剂治疗,血压控制在160/90 mmHg左右。近2个月血压失控,收缩压飙升至180-200 mmHg,无活动后下肢无力、胸痛或呼吸困难症状,易自觉燥热、面部潮红,伴下肢水肿。8年前曾有脑出血病史,家族中有多名早发高血压患者。
关键线索:血钾同样偏低(3.2 mmol/L),ARR 85.9。入院生理盐水负荷试验阳性,(试验后,血浆醛固酮121.4 pg/ml)。完善肾上腺增强CT提示左侧醛固酮瘤。
诊断:醛固酮瘤(APA)。接受腹腔镜下肾上腺切除术后,血压和血钾恢复正常。
阵发性房颤、脑出血、难治性高血压,看似是心、脑、血管三个层面的独立问题,但抽丝剥茧后,它们共同的病理生理基础均指向——原发性醛固酮增多症,可视为明确的醛固酮失调。这提示临床,对于合并阵发性心房颤动、脑出血或难治性高血压的患者,需警惕醛固酮失调在背后作祟。
二、跨界寻踪:
醛固酮失调与“心-脑轴”的隐秘联动
传统认知中,“心-脑轴”的关联仅被归结为脑血管意外与心血管疾病拥有共同危险因素(如高血压、糖尿病等代谢异常),以及心源性脑卒中与应激性心肌病相关。但事实真的仅止于此吗?为何醛固酮失调会同时累及心脏与大脑?
1.醛固酮失调
醛固酮可通过两种途径发挥生物学效应:一是盐皮质激素受体(MR)途径——作用于MR,经数小时至数天的转录-翻译响应起效,受体分布于远端肾小管上皮及心脏、血管平滑肌、大脑等组织;二是非MR途径——作用于GPER等受体,呈秒至分钟级快速响应,受体分布于血管内皮、平滑肌、心肌等多类组织。
一项纳入1688例非高血压患者、中位随访4年的前瞻性研究显示,血清醛固酮水平与血压升高及高血压发病直接相关:以最低四分位数组为参照,最高四分位数组的血压升高风险增加60%、高血压发病风险增加61%(图1)[1]。
目前,业内,对醛固酮失调的定义不明晰。但原发性醛固酮增多症可被视为最典型的醛固酮失调的疾病。
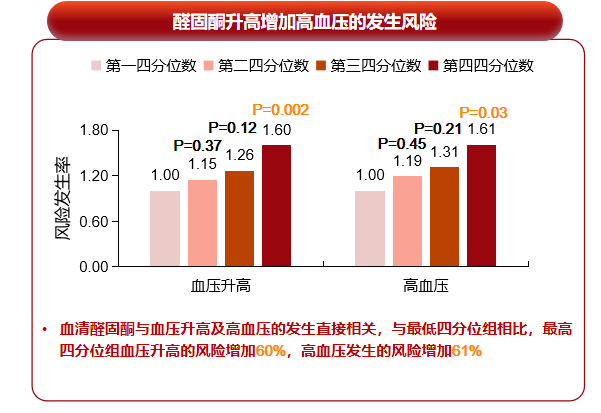
图1. 醛固酮升高增加高血压的发生风险
2.原发性醛固酮增多症
原发性醛固酮增多症(PA)由肾上腺过度分泌醛固酮所致:过量醛固酮激活远端肾小管上皮细胞的MR,上调上皮钠通道(ENaC)表达,进而促进钠重吸收与钾排泄,引发血压控制不佳、低钾血症、水肿等表现。由于该病缺乏特异性临床特征,临床筛查率不足1%[2]。
过量醛固酮与钠负荷可导致心肌肥厚、肾功能损伤。与原发性高血压患者相比,PA患者发生心房颤动、卒中、冠心病、心力衰竭的风险显著更高[3]。
3.心脑轴:从临床现象到基础机制
心脑之间联系紧密,这一观点早已得到临床观察的证实。例如,超过60%的急性缺血性卒中患者会在发病24小时内出现心电图改变,包括QT间期延长、ST段改变等。在小鼠心肌梗死(MI)模型中,也有相关现象佐证这种联系:经TSPO放射性示踪剂检测到的神经炎症情况,与小胶质细胞免疫荧光染色结果一致。而且,这种神经炎症会先短暂消退,在慢性心力衰竭阶段再次出现,此时其严重程度与心脏收缩功能呈负相关[4]。
目前,针对MI状态下的神经和神经免疫机制研究尚不充分。不过,借助scRNA-seq和组织透明化技术,研究发现TRPV1迷走神经感觉神经元(VSNs)增加了对心室的神经支配,而消融VSNs能够减少梗死面积,降低促炎细胞因子IL-1β的水平,追溯至大脑层面,发现MI时,下丘脑室旁核(PVN)中表达血管紧张素II受体1型的神经元表达增加,并且抑制这些神经元所产生的效果,与消融TRPV1VSNs的益处相似。此外,研究还发现颈上神经节(SCGs)在MI后出现变化,其交感神经支配增强,同时IL-1β信号传导也增强。而阻断SCG中的IL-1β,可显著减少MI后的并发症[5]。
4.新假说:心房是心脑对话的关键“中转站”?
学术界注意到,心房心肌病(无论是否合并房颤)会增加卒中、无症状性脑梗死及痴呆的发病风险。这引发了新的思考:心房功能异常导致脑血管损伤的机制,是否超越了微血栓脱落,涉及更为复杂的炎症反应?由此,一个极具价值的科学假说被提出:“醛固酮失调→左房功能异常(LA dysfunction)→脑功能失调/脑血管意外”。这一神经心脏病学视角的传导链条,为未来的临床研究提供了新方向。
三、破局之道:
精准诊疗,阻断心脑损害链条
面对醛固酮失调带来的系统性损害,早期筛查与精准治疗是改善“心-脑”预后的关键。
1.精准筛查:锁定高危人群
由于PA缺乏特异性体征,且临床筛查率不足1%,扩大高危人群筛查范围至关重要。除传统的难治性高血压患者、合并低钾血症的高血压患者外,以下人群也应纳入PA筛查范畴:合并房颤的高血压患者(尤其是孤立性房颤)[6]、有脑出血病史的高血压患者、有早发高血压家族史或脑卒中家族史的高血压患者。对这类人群常规开展醛固酮/肾素活性比值(ARR)检测,是发现潜在PA患者的第一步。
2.分型施治:手术与药物的双重策略
一旦确诊PA,需根据分型采取个体化治疗方案(表1)。对于单侧病变(如醛固酮瘤APA、单侧肾上腺增生UAH),腹腔镜下肾上腺切除术为首选方案,有望实现临床治愈,使血压和血钾恢复正常(如前述病例2);对于双侧病变(特发性醛固酮增多症IHA)或无法/不愿接受手术的患者,盐皮质激素受体拮抗剂(MRA)是一线治疗药物,螺内酯、依普利酮等可竞争性抑制醛固酮受体,在降低血压的同时保护靶器官。
表1. PA的分型与治疗策略

3.前沿展望:从源头抑制醛固酮合成
除阻断受体外,直接从源头抑制醛固酮合成是另一条颇具前景的新方向。Bax24研究显示,针对难治性高血压患者,采用高选择性醛固酮合成酶抑制剂Baxdrostat(2 mg/日)治疗12周后,效果显著:血清醛固酮水平大幅降低76%,24小时动态收缩压显著下降16.6 mmHg,血压达标率(<130 mmHg)高达70.6%[7]。
结语
跳出“头痛医头、脚痛医脚”的传统诊疗框架,从神经心脏病学的视角审视,醛固酮失调绝非仅关乎血压与血钾数值的问题——它是串联心脏重塑(如房颤、心衰)与脑血管损伤(如卒中)的关键枢纽。识别并干预这一病理过程,为心脑血管疾病的综合防治开辟了新的路径与策略。

专家简介
包丽雯
复旦大学附属华山医院
复旦大学附属华山医院心内科副主任医师、医学博士。
华山临床医学院内科学教研室副主任。
华山医院心电图室(心血功能室)主任。
2024年美国麻省总院访问学者,2018-2019年参与哈佛大学医学院全球临床研究者培训。
中国医师协会第六届罕见心血管病专业委员会委员,中国高血压联盟理事,中国心血管代谢联盟青年委员会秘书长,中国疾控预防中心心力衰竭全程管理中心青年委员,上海市医学会心血管病分会心脏康复学组委员,上海市康复医学工程研究会心血管病临床研究专委会委员,中国微循环学会基层慢病管理委员会委员。
参考文献:
1.N Engl J Med. 2004;351:33-41.
2.Circulation. 2018 Aug 21;138(8):823-835.
3.Lancet Diabetes & Endocrinology, 2017, 6(1): 41.
4.J Nucl Cardiol. 2024 June
5.Cell. 2026 Feb 5;189(3):800-817.e20.
6.Milliez P. et al. JACC 2005;45: 1243–8
7.Williams B, et al. AHA Congress 2025.

我要留言