编者按:
在心血管医生的诊室里,最让人头疼的不是不吃药的患者,而是那些遵医嘱服药但血压依然岿然不动的患者。这种现象,我们称之为“难治性高血压”。难道人类的降压治疗真的存在一层无法逾越的“天花板”吗?
近日,在2026年美国心脏病学会年会(ACC.26)上,Luke Laffin教授带来了关于新型降压药物Tonlamarsen的KARDINAL Ⅱ期研究最新结果,试图为我们揭开谜底。该研究成果同步发表在Journal of the American College of Cardiology。



什么是降压“天花板效应”?——当人体启动了代偿机制


所谓降压的“天花板效应”,是指在高血压治疗中,随着药物种类和剂量的不断增加,血压下降幅度却逐渐趋于平缓甚至停滞,同时副作用开始反扑。
这背后的原因是人体的代偿机制:当用ACEI堵住了A通道,机体会选择绕过该通道,通过B途径(例如,非ACE途径产生的血管紧张素Ⅱ)或者通过反射性提高心率、增加钠水重吸收来维持血压。这种“你追我赶”的博弈,使得传统药物在进入多药联用阶段后,往往陷入了“加药不降压”的泥潭。

治疗困境:难治性高血压引发的恶性循环


目前难治性高血压的治疗面临巨大挑战,患者在长期降压治疗中,最隐性的代价是药物不断叠加所引发的副作用,以及由此导致的依从性下降所形成的恶性循环。
多种药物叠加给患者带来的负担相当沉重,例如,利尿剂可能引发电解质紊乱,钙通道阻滞剂常导致下肢水肿,而多药联用还可能造成肾功能波动。这种治疗模式不仅增加了生理风险,也显著降低了患者的生活质量。
更重要的是,这种复杂的用药方案对依从性提出了极高要求。每天需要精确服用四到五种药物的患者经常会有持续的紧张与不确定性,这也往往成为压垮依从性的最后一根稻草。
从机制上看,肾素-血管紧张素-醛固酮(RAS)系统是人体血压调控的“中枢指挥系统”。目前主流的降压药物,如ACEI和ARB,主要作用于RAS系统的中下游环节。这类似于在河流中游筑坝:如果上游水源持续不断,下游的阻断终究存在被“溢流”的风险。
因此,研究者逐渐将目光转向更上游的调控环节——由肝脏合成的血管紧张素原(AGT)。通过在源头减少底物供给,或许可以从根本上阻断RAS系统的过度激活,从而为难治性高血压提供一种全新的治疗路径。

什么是AGT?揭秘血压调节的“源头活水”


如果把人体调节血压的RAS系统比作一条精密运行的“升压物质生产线”,那么AGT就是这条生产线上最源头、最基础的“原材料”。AGT主要由肝脏合成并释放到血液中,其本身并无升压作用,但通过以下两步“变形”后,演变成了血压的幕后推手:
第一步(裁剪):当血压下降时,肾脏会分泌一种叫“肾素”的酶。它像一把精准的剪刀,将血液中的AGT剪开,转化为血管紧张素Ⅰ。
第二步(激活):血管紧张素Ⅰ在转换酶的作用下,进一步蜕变为强大的血管紧张素Ⅱ。这才是导致血管剧烈收缩、血压飙升的“罪魁祸首”。

“源头截流”即可大力出奇迹?未必!


KARDINAL 研究提出了一种具有颠覆性的治疗假设:与其在RAS系统的下游反复“筑坝控流”,不如在源头直接“釜底抽薪”,从根本上减少升压信号的产生。
基于这一思路,研究引入了一种创新性的反义寡核苷酸药物——Tonlamarsen。该药物能够选择性进入肝细胞,通过干扰AGT的基因表达,从源头抑制其合成过程,实现对RAS系统的上游调控。
为了验证该假设,研究共纳入198例难治性高血压患者。所有入组患者在联合使用2~5种降压药物(其中超过80%已包含ACEI或ARB)的情况下,诊室收缩压仍高于135mmHg,提示常规治疗控制不佳。
研究采用随机、双盲、安慰剂对照设计。所有患者在导入期均接受一次Tonlamarsen注射,随后按随机分配进入Tonlamarsen治疗组或安慰剂组,干预持续20周(见图1)。
主要终点为评估干预前后血浆AGT水平及收缩压(SBP)的变化,以反映药物对 RAS 系统源头调控及降压效果的影响。次要终点包括安全性评估、动态血压监测结果,以及单次给药与多次给药方案之间疗效差异的比较。
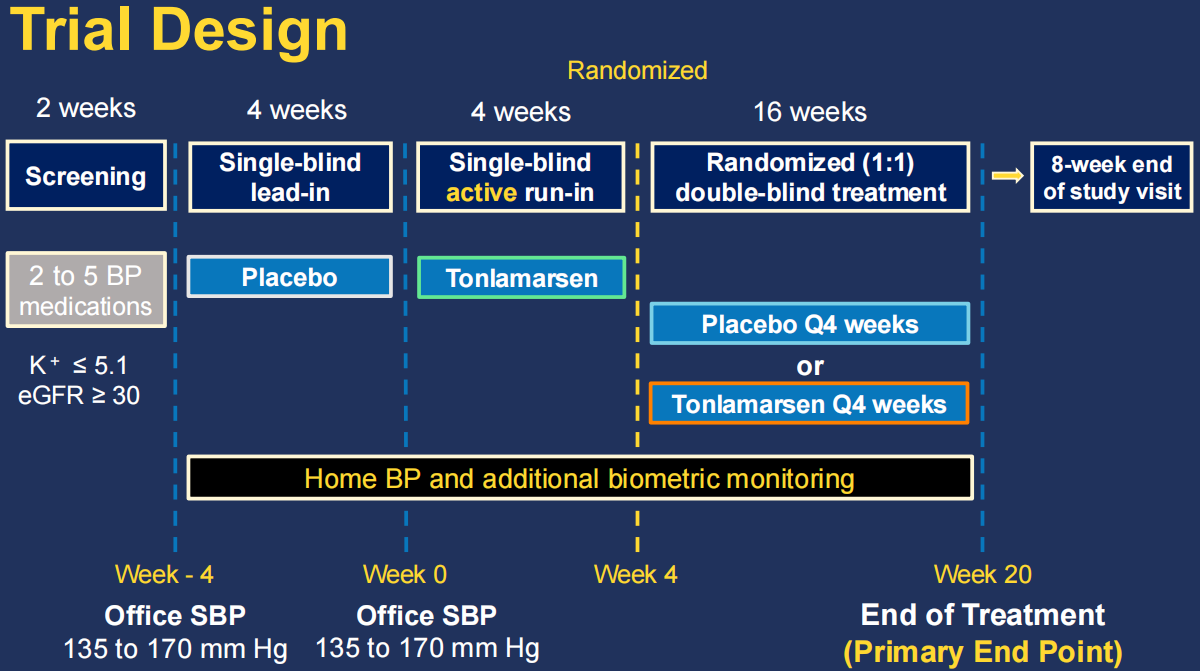
图1. KARDINAL 研究设计
研究结果发现:
与安慰剂组相比,Tonlamarsen治疗组的血浆AGT水平显著降低了67.2%(图2)。
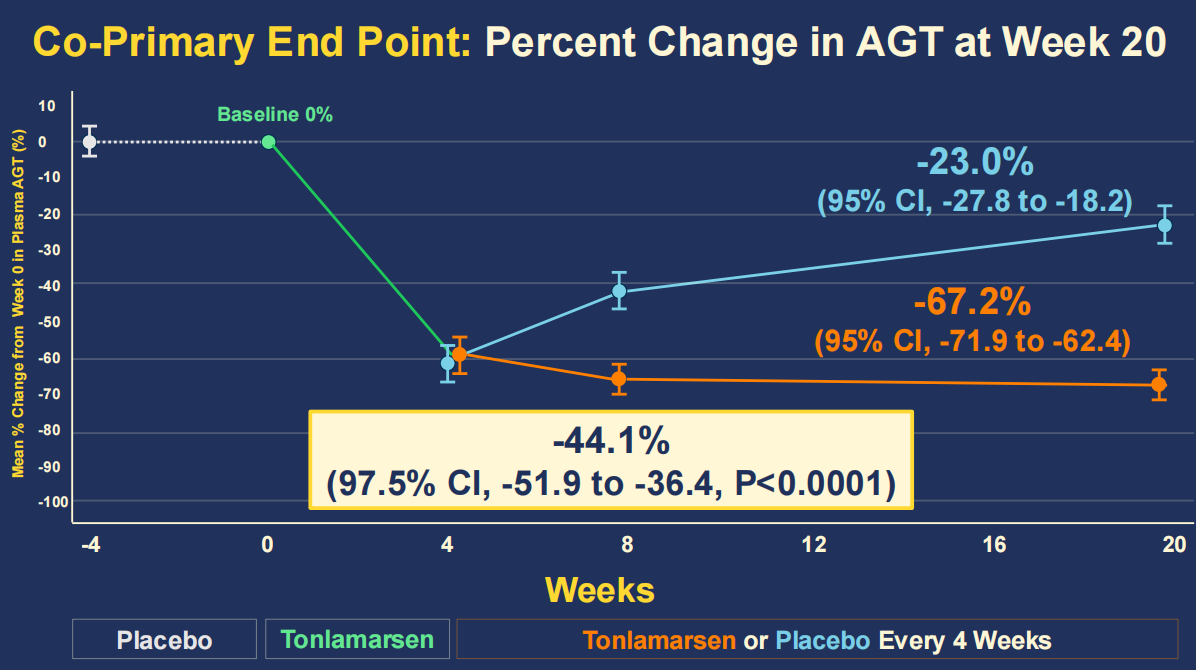
图2. Tonlamarsen治疗组与安慰剂组的血浆AGT水平变化
两组的诊室收缩压(SBP)降幅无统计学上差异(图3)。
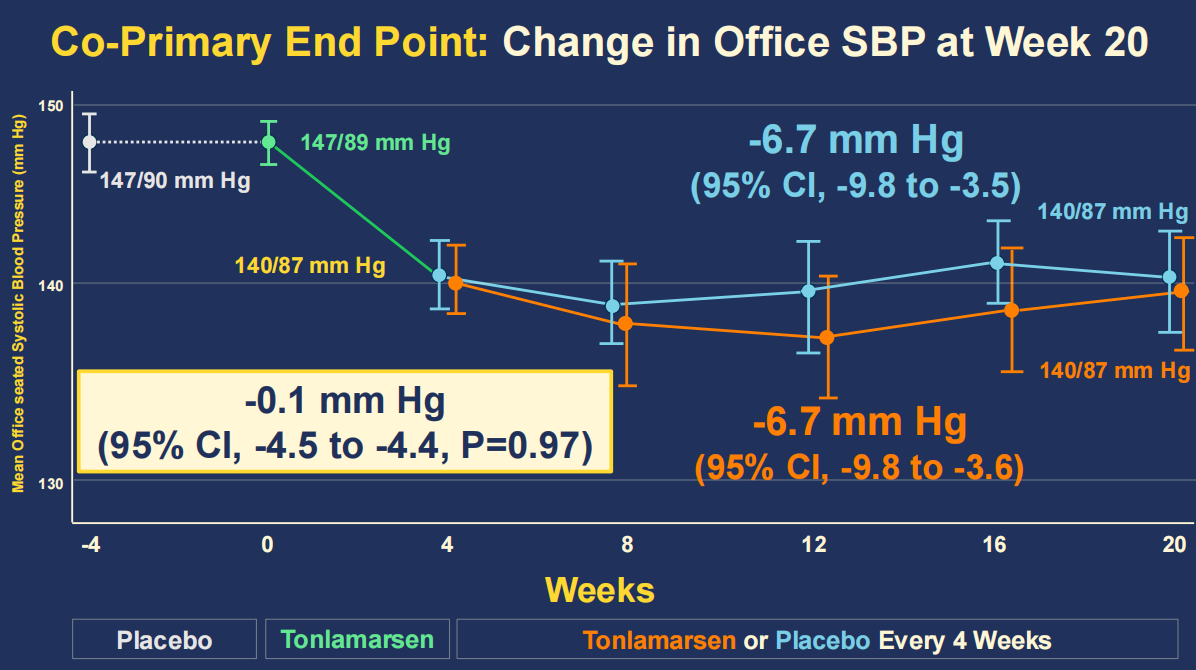
图3. Tonlamarsen 治疗组与安慰剂组的诊室收缩压(SBP)变化
安慰剂组的患者中(在导入期接受过一次Tonlamarsen单剂量给药),其AGT水平在20周后依然保持了约23%的残余抑制。
在为期5个月的治疗过程中,Tonlamarsen表现出良好的安全性,未观察到严重的电解质紊乱或与药物相关的显著不良事件(表1)。
表1. Tonlamarsen 治疗组与安慰剂组的不良事件发生率
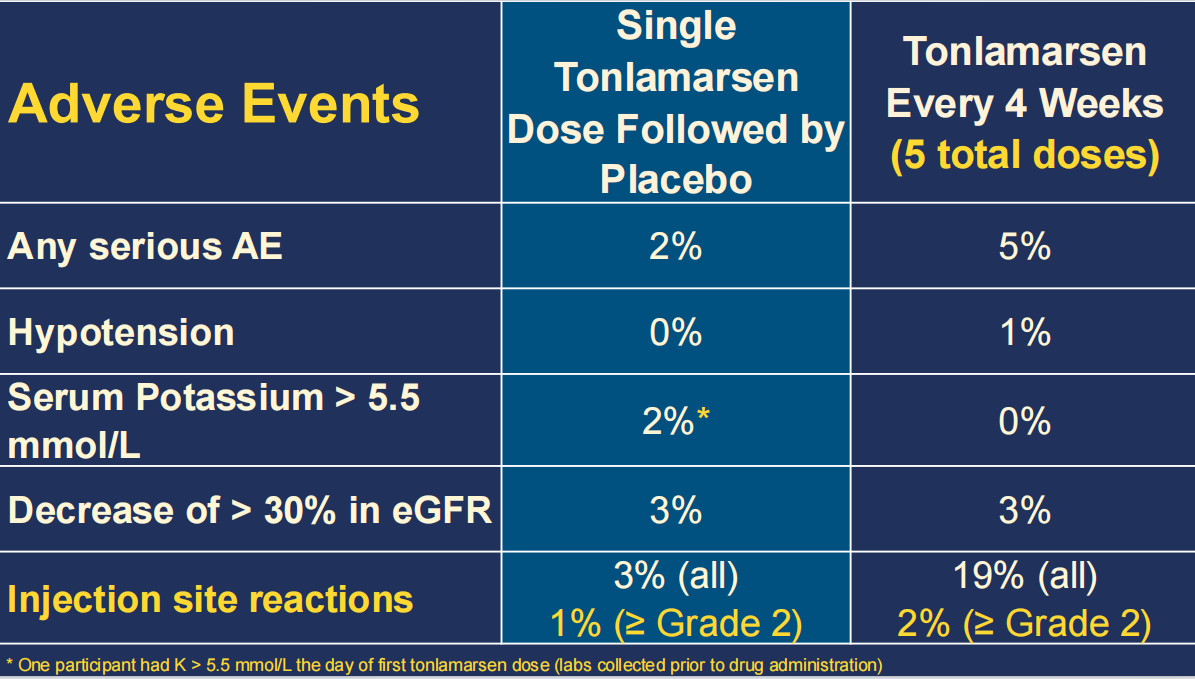
简而言之,KARDINAL试验证实:在已经联用多种药物的顽固性高血压患者中,Tonlamarsen可以有效地降低血浆AGT水平,但未显著降低患者的SBP。

为何“源头截流”未能实现显著降压?


尽管KARDINAL研究表明,Tonlamarsen在机制上实现了对AGT的显著抑制,但其降压效果并未呈现出预期效果。作者认为原因可能有以下几方面:
1.入组患者均为接受2~5种降压药的难治性高血压人群,ACEi/ARB等药物已阻断RAAS下游通路,大幅削弱了抑制上游AGT的潜在降压作用;
2:Tonlamarsen产生了意料之外的AGT持久抑制作用,导致安慰剂组在单次给药后20周仍存在残留降压效应,掩盖了治疗组多次给药的降压作用。
3:Tonlamarsen单次AGT抑制作用触发了机体的长期生理代偿,无需持续抑制即可维持降压效果,导致持续每月给药无法产生额外作用。

“意外收获”:从疗效强度到疗效持续性的转变


尽管Tonlamarsen的降压效果并未突破难治性高血压的“天花板效应”,但研究也揭示了一个具有潜在变革意义的发现,即Tonlamarsen通过抑制AGT合成可能带来显著而持久的降压作用。
研究显示,即便在停止给药后,Tonlamarsen对AGT的抑制作用仍可持续数月。这种“长效源头控制”的特性,为高血压治疗提供了新的可能路径——对于部分患者,未来或可通过“季度一次”甚至“半年一次”的给药方式,实现对血压的长期稳定控制,从而减少对每日口服多种药物的依赖。
这一模式的转变,不仅有望改善治疗依从性,也可能在一定程度上重塑高血压的长期管理策略。

小结:


KARDINAL Ⅱ 期临床试验探索了从RAS系统上游抑制AGT合成对难治性高血压的治疗作用。尽管Tonlamarse实现了血浆AGT水平的显著降低且药物安全性良好,但未展现出显著的降压效果。然而,研究却发现该药物对AGT的抑制具有长效性,为高血压长效治疗、提升患者治疗依从性提供了新的探索方向。
参考文献:
1.Laffin LJ, et al. Efficacy of tonlamarsen in patients with uncontrolled hypertension: the KARDINAL phase 2 randomized clinical trial. J Am Coll Cardiol. 2026. doi:10.1016/j.jacc.2026.03.034
2.Efficacy and Safety of Tonlamarsen in Patients with Uncontrolled Hypertension.American College of Cardiology 2026, Scientific Sessions, Late-Breaking Clinical Trial. March 28, 2026

我要留言