编者按
髋部骨折常被称为“老年人最后一次骨折”,其伴随的高死亡率与高致残率已成为严重的公共卫生问题。传统康复手段虽能在一定程度上恢复功能,但对骨折后迅速发生的身体成分恶化——特别是内脏脂肪的异常积累——往往效果有限。随着全球人口老龄化趋势加剧,如何有效改善这一高危人群的代谢健康显得尤为紧迫。
近期,STEP-HI研究结果的发表为这一难题提供了新思路。这项研究显示,在常规运动康复基础上联合外源性睾酮治疗,可能通过调整脂肪分布而减少内脏脂肪比例,为改善老年髋部骨折女性的代谢健康带来新的路径。研究的相关结果近日发表在Innovation in Aging,不仅为老年女性的睾酮治疗提供了重要临床证据,也为多学科协作的康复模式注入了新的研究方向。


老年髋部骨折:不止是骨骼的危机
髋部骨折对老年女性而言是一场全身性危机。研究显示,高达76%的患者会经历长期健康问题与功能衰退。此外,骨折后的活动受限和炎症加剧可导致肌肉快速流失(少肌症),同时脂肪向内脏区域异常积聚。这种“脂肪转移”并非简单的体重增加,而是代谢风险的质变——因为内脏脂肪是高度活跃的“内分泌器官”,可持续分泌炎症因子,加剧胰岛素抵抗,增加动脉粥样硬化和再次跌倒骨折的风险。
传统的康复训练虽可改善肌力与平衡,但对这种异常的脂肪分布束手无策。性激素——尤其是睾酮——在调节脂肪分布中扮演着关键角色。在男性中,年龄相关的睾酮下降与内脏脂肪增加密切相关,而补充睾酮已被证明可以改善脂肪分布,减少内脏脂肪比例。在女性中,随着年龄增长和绝经,雌激素下降同样会导致脂肪向内脏转移,但睾酮对女性体脂分布的作用此前研究甚少且结论不一。
既往的观察性研究提示,绝经后女性的内源性睾酮水平与某些心血管健康标志物呈正相关。尽管从生物学机制上看,睾酮具有合成代谢(促进肌肉)和脂解作用(减少脂肪),且内脏脂肪组织因含有更高的雄激素受体、细胞密度、神经支配和血流量,可能对睾酮更为敏感,但相关临床研究长期缺失。
在此背景下,研究者们提出了一个科学假设:在运动康复基础上加入睾酮治疗,可能比单纯运动更能促进脂肪健康分布,降低内脏脂肪的相对比例,从而为改善代谢健康与长期预后提供新的治疗策略。STEP-HI研究首次在髋部骨折后老年女性这一高危群体中,系统探索将睾酮治疗与结构化运动康复相结合的方案,试图从激素层面改善身体成分的分布,特别是扭转不利于代谢健康的内脏脂肪积聚趋势。

STEP-HI研究:一项范式创新的临床试验
STEP-HI研究是一项多中心、双盲、随机对照试验,纳入66例平均年龄78岁、睾酮水平偏低(≤60 ng/dl)的髋部骨折术后老年女性。所有参与者被随机分为两组:结构化运动康复+睾酮凝胶组(EX+T组,目标血药浓度110~160 ng/dl)及结构化运动康复+安慰剂凝胶组(EX+P组)(图1)。结构化运动康复包括力量、平衡与功能训练。
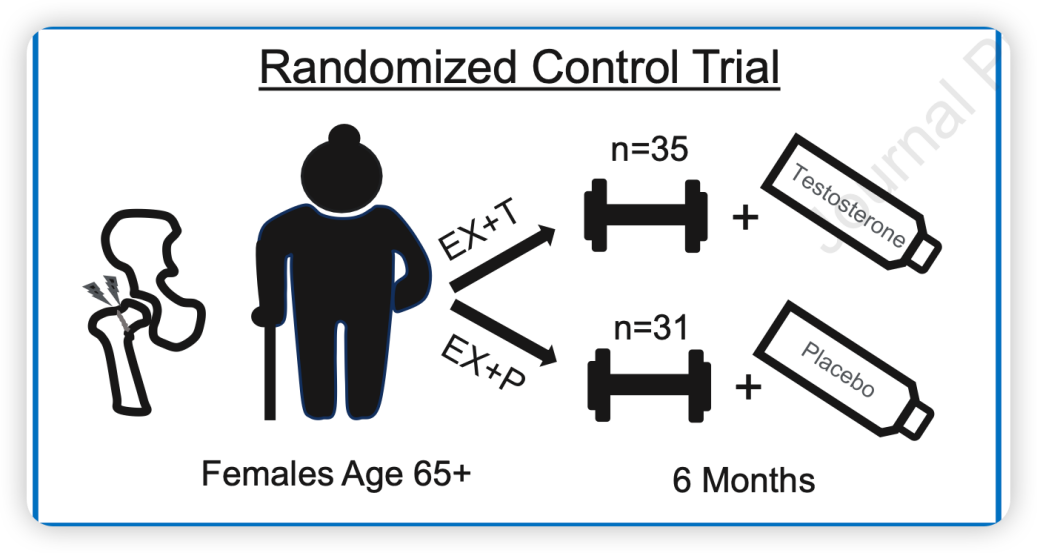
图1.随机分配为两组
在接受为期6个月的干预治疗前后,研究者采用双能X线吸收测定法(DXA)精确评估参与者的脂肪分布变化。结果出人意料又振奋人心:虽然总脂肪未减,但“脂肪地图”被重绘。
具体地看,两组的总脂肪量(TAT)均未显著减少,然而,EX+T组的相对内脏脂肪比例(%VAT)较基线显著降低10.57%,而安慰剂组反而上升3.51%,因此两组的差异高达14.08%(图2)。这意味着脂肪从高风险的“内脏仓库”向相对安全的皮下区域迁移。
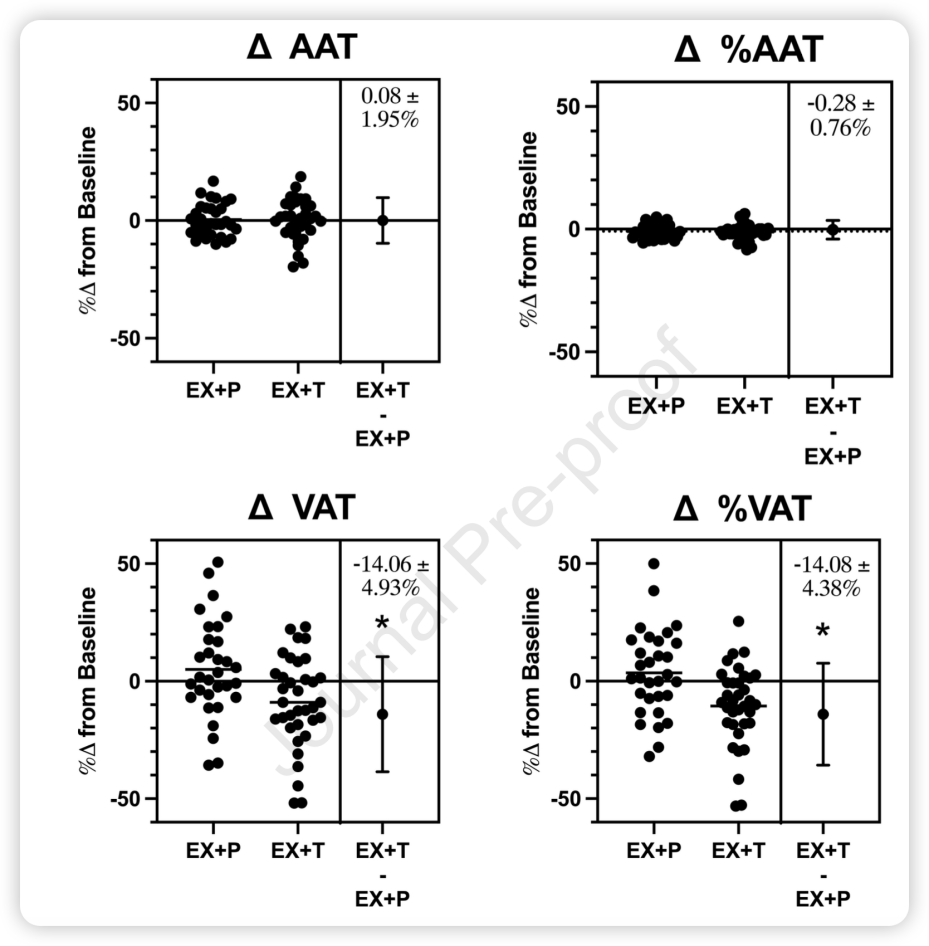
图2. EX+T组及 EX+P组,基线及干预后内脏脂肪绝对量(VAT)、四肢脂肪绝对量(AAT)、内脏脂肪相对比例(%VAT)及四肢脂肪相对比例(%AAT)的变化情况。* 表示组间差异具有统计学意义。

机制探秘:为什么睾酮能改变脂肪分布?
脂肪组织不仅是能量储存库,更是一个布满激素受体的活跃内分泌器官。研究表明,内脏脂肪组织(VAT)相较于皮下脂肪,其雄激素受体表达更高、细胞密度更大、血供与神经支配更丰富,因而对睾酮的作用反应尤为敏感。睾酮可能通过以下多重机制,选择性调节脂肪分布,尤其是减少内脏脂肪比例:
增强区域性脂解作用
睾酮可激活脂肪细胞内的脂解通路。研究指出,睾酮对内源性脂解活性的促进作用在内脏脂肪中比在皮下脂肪中更为显著。这可能是由于内脏脂肪中有更高的肾上腺素能受体密度与激素敏感性脂酶活性所致。
抑制脂肪形成与分化
雄激素能调控前脂肪细胞向成熟脂肪细胞的分化过程。证据显示,睾酮可降低脂肪生成相关转录因子(如PPARγ、C/EBPα)的表达,从而抑制新的脂肪细胞生成,且该效应在内脏脂肪库中更为明显。
调节炎症与代谢微环境
内脏脂肪是慢性低度炎症的主要来源,其分泌的促炎细胞因子会加剧胰岛素抵抗和代谢紊乱。睾酮可能通过下调内脏脂肪中巨噬细胞浸润及促炎因子(如TNF-α、IL-6)的表达,改善局部炎症状态。此外,相对内脏脂肪比例(%VAT)本身即是比单纯脂肪总量更强的心代谢风险预测指标。
在老年女性髋部骨折后的特殊生理阶段,机体常处于“高分解代谢”与“高炎症”的双重压力之下,脂肪异常向内脏积聚的风险显著增加。此时,外源性睾酮的介入,恰似一个“代谢重塑的助推器”——它可能通过上述机制,优先作用于内脏脂肪库,促进脂肪从内脏区域向其他代谢相对惰性的部位再分布,从而在不显著改变总体脂肪量的情况下,优化脂肪分布格局,改善代谢健康前景。

研究意义:重新定义老年康复的边界
既往观察性研究曾提示睾酮可能与女性内脏脂肪积累相关,而单纯运动的改善作用有限。然而,本项随机对照研究首次证实,对于睾酮水平偏低且处于髋部骨折恢复期的老年女性而言,外源性睾酮联合系统康复运动能够实现与男性相似的“脂肪健康再分布”效应。这一重要发现揭示出,激素作用的效果高度依赖于机体的具体生理与代谢状态,具有显著的情境依赖性。
更值得关注的是,运动与睾酮干预在此过程中展现出明确的协同机制。一方面,运动为激素调控营造了适宜的代谢与细胞环境;另一方面,睾酮则进一步增强了运动对脂肪分布——尤其是内脏脂肪比例——的定向调节能力。两者相互促进,共同推动身体成分向更健康的结构模式重构。
该研究为特定高危人群的代谢健康管理提供了新的临床思路。针对髋部骨折后内脏脂肪异常积聚风险较高且伴低睾酮水平的老年女性,可在规范化康复训练的基础上,在严密监测下实施个体化、低剂量的睾酮补充治疗,以优化体脂分布、改善代谢功能及长期预后。未来研究需进一步明确治疗的最佳剂量窗口、干预周期与长期安全性,并探索该联合策略在老年衰弱综合征及其他代谢相关疾病群体中的适用价值。
此外,STEP-HI研究结果也进一步证实,即使在高龄与重大创伤后,人体仍具备明显的代谢与形态可塑性。这提示未来老年医学的发展重点,应从泛泛的“抗衰老”转向精准的“代谢调节”——即在恰当时机,通过科学手段引导机体成分向更健康的方向演进。
总体而言,当激素疗法与系统化康复手段深度融合,我们见证的不仅是脂肪分布的有益改变,更是老年健康管理模式的一次重要演进。这也标志着,临床实践正逐步从被动应对疾病转向主动构建并维持功能与代谢健康的新阶段。
参考文献:Earp, J., Zhao, S., Xu, F., Fortinsky, R., Bartley, J., Kuo, C. L., & Kuchel, G. (2025). Testosterone Therapy Effects Adipose Distribution in Older Females Post Hip-Fracture: The STEP-HI Study. Innovation in Aging, 9(Suppl 2), igaf122.4021. https://doi.org/10.1093/geroni/igaf122.4021

(来源:《减重时讯》编辑部)

我要留言