引言:

2023年,美国心脏协会提出了心血管-肾脏-代谢(CKM)综合征的概念,旨在帮助临床医生整合分析心血管、肾脏与代谢系统之间交互作用的共同病理生理机制,从而更精准地评估症状、体征、靶器官损害、心血管发病风险及死亡风险,并指导治疗决策。在CKM综合征范式下,慢性肾病的管理应被高度重视。
在第75届美国心脏病学会科学年会(ACC.26)上,来自美国杜克大学医学院的Daniel Edmonston医生,从肾脏科医生的视角出发,强调慢性肾病管理对于降低心血管疾病风险的显著获益。《心肾代谢时讯》特邀我国著名肾内科专家——广东省人民医院梁馨苓教授对此深入解读。

01
慢性肾病的最大担忧并非肾衰竭,而是心血管风险!
许多临床医生和患者往往误以为慢性肾病的主要结局是肾衰竭。然而事实恰恰相反,慢性肾病患者的心血管疾病及其死亡风险远高于进展至肾衰竭的风险。即使处于早期慢性肾病(1~3期),患者的心血管事件发生率已显著高于普通人群;而到了晚期慢性肾病(4~5期),心血管风险更是急剧升高。心血管疾病而非终末期肾病是这一高危人群的主要死亡原因。Daniel Edmonston医生指出,需要透析治疗的年轻慢性肾病患者,其心血管死亡风险仍然远高于不合并慢性肾病的老年人群。
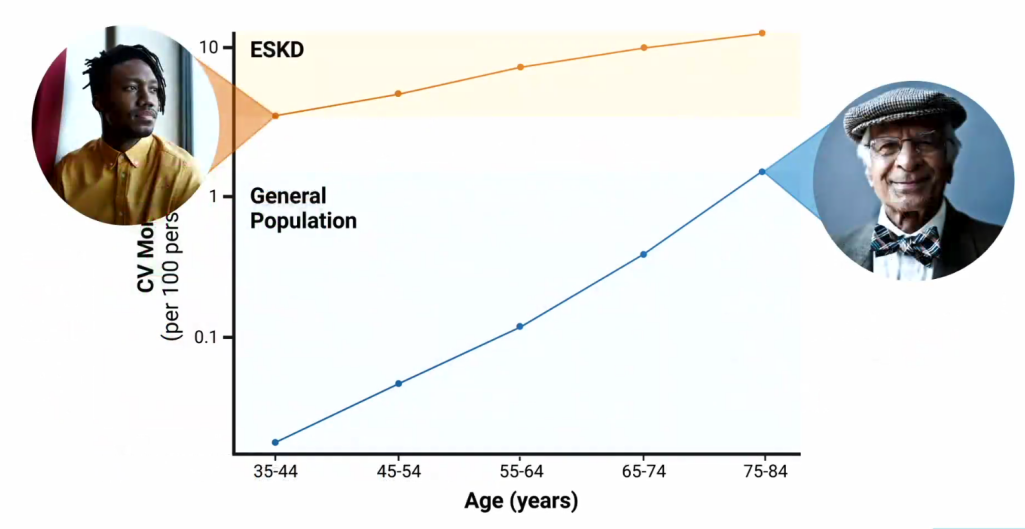
图1. 终末期肾病与普通人群心血管死亡风险对比
病理生理机制上,慢性肾病可引起全身性、慢性的促炎状态,促进血管和心肌的重塑过程,导致动脉粥样硬化病变、血管钙化、血管衰老,以及心肌纤维化和心脏瓣膜钙化。从这个角度看,慢性肾病相当于加速了心血管系统的衰老。研究显示,随着慢性肾病的分期增加,患者心血管疾病(如:左心室肥厚、肺动脉高压、心房颤动、动脉粥样硬化性心血管疾病、心力衰竭)的发生风险不断提升。
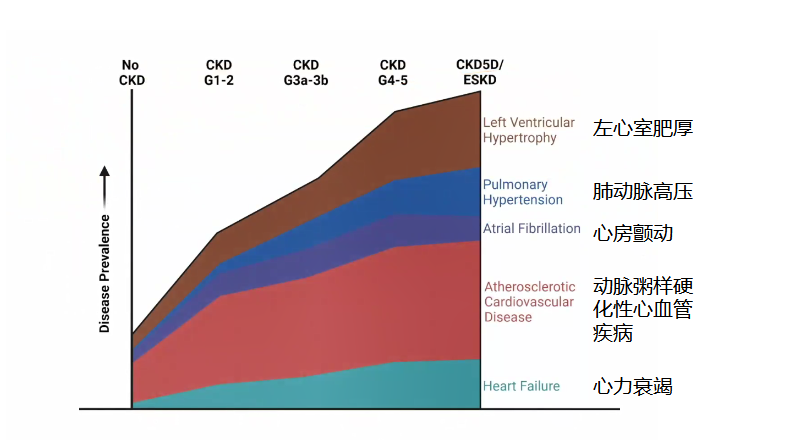
图2. 不同分期慢性肾病心血管并发症风险
对于慢性肾病患者而言,其心血管风险来自包括糖尿病、高血压、血脂异常、肥胖、吸烟在内的这类传统因素,此外还包括了与慢性肾病相关的特定风险因素:尿毒症、矿物质代谢紊乱、贫血以及容量负荷过重。
02
一旦发现肾病即进入CKM综合征范式
CKM综合征根据代谢风险、慢性肾病分期及心血管病变程度分为多个阶段。
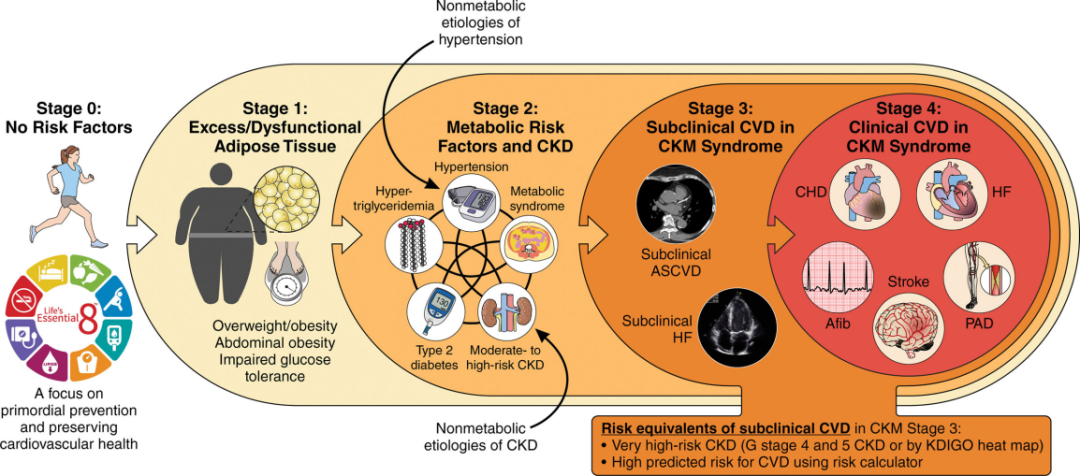
图3.CKM综合征病程分期与病理机制
CKM 0期:包括体重正常、血糖正常、血压正常、血脂正常、肾功能正常,且无亚临床或临床心血管疾病证据的个体。0期的重点是原始预防和维持心血管健康。
CKM 1期:包括存在脂肪组织过多、脂肪组织功能异常或两者兼有的个体。
CKM 2期:包括存在代谢危险因素(高甘油三酯血症、高血压、代谢综合征或2型糖尿病)、中高危慢性肾脏病或两者兼有的个体。
CKM 3期:包括存在亚临床心血管疾病并伴有CKM危险因素(脂肪过多/功能异常、代谢危险因素或慢性肾病)的个体,或存在极高危慢性肾病这一风险等效因素,或CKM风险计算器预测为高风险的个体。
CKM 4期:包括存在临床心血管疾病(冠心病、心力衰竭、卒中、外周动脉疾病或心房颤动)并伴有CKM危险因素的个体。
在CKM综合征范式中,中高危慢性肾病对应的是CKM2期,而极高危慢性肾病对应CKM3期。估算肾小球滤过率(eGFR)和尿微量白蛋白肌酐比值(UACR)是慢性肾病分期的两大核心指标,同时也是患者发生心血管事件或心血管死亡的独立危险因素。通过这两大指标的评估,一旦发现尿液白蛋白异常升高,即标志着患者已进入CKM综合征,需启动综合管理。
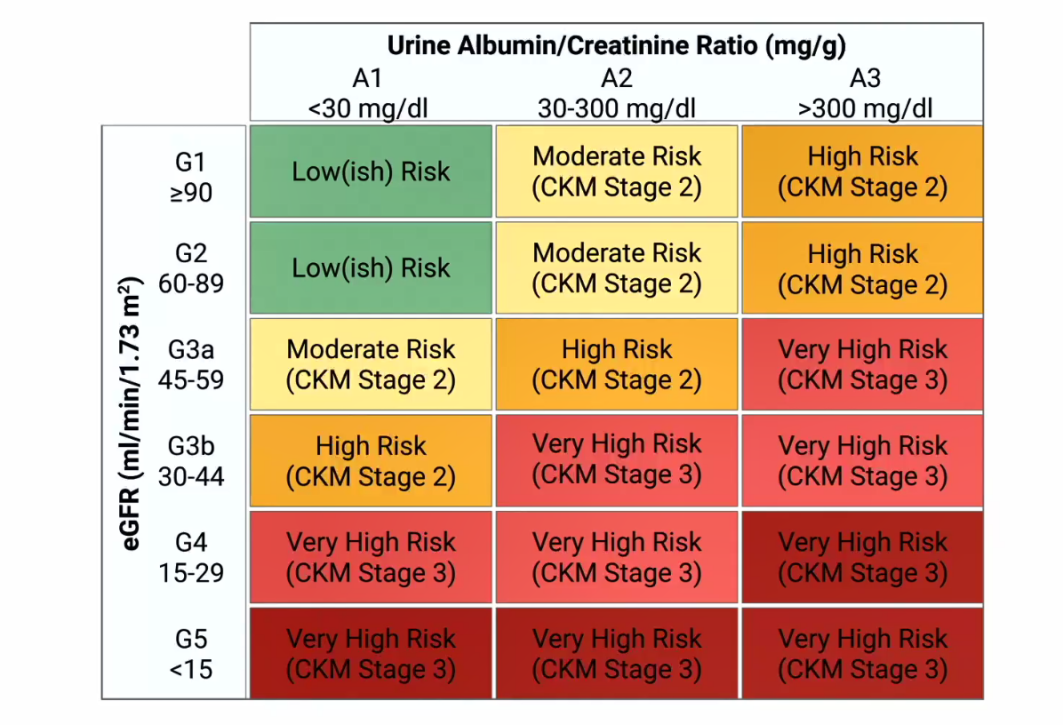
图4. 基于eGFR与UACR的CKD风险分层及CKM分期
03
降低慢性肾病进展及心血管风险的4大类药物
根据指南指导的药物治疗,目前已有四类药物被证实可延缓慢性肾病进展并降低心血管事件风险:
1)肾素-血管紧张素系统抑制剂(RASi):
可降低约26%心力衰竭发生率;轻微降低心肌梗死、卒中的发生率;其对外周动脉疾病的获益未知;观察性研究发现可降低心房颤动风险。
2)钠-葡萄糖共转运蛋白2抑制剂(SGLT2i):
可降低50%心力衰竭发生率,并降低47%的心房颤动发生率;轻微降低心肌梗死、卒中的发生率;其对外周动脉疾病获益未知。
3)非甾体类盐皮质激素受体拮抗剂(nsMRA):
可降低32%心力衰竭发生率;降低14%主要不良心血管事件(MACE)发生率,但具体对于心肌梗死、卒中的影响未可知;此外可降低17%心房颤动发生率;其对外周动脉疾病获益未知。
4)胰高血糖素样肽-1受体激动剂(GLP-1RA):
可降低28%心力衰竭发生率;降低22%MACE发生率,但具体对于心肌梗死、卒中的影响不清楚;其对心房颤动、外周动脉疾病获益未知。
专家点评
梁馨苓教授:
广东省人民医院

Daniel Edmonston教授从肾脏科医生的视角出发,对CKM综合征进行了系统而深入的剖析。本次讲座的重要价值之一,在于推动对慢性肾病(CKD)结局认知的再校正,并进一步凸显CKM综合征框架在临床管理中的重构意义。
长期以来,无论临床医生还是患者,往往将肾衰竭视为CKD的主要结局,治疗重点亦集中于延缓透析或肾移植的发生。然而,CKD患者更主要的威胁实际上来源于心血管事件及其相关死亡,这一观点具有重要的临床警示意义。但我们也需要认识到,这种认知转变并不意味着可以弱化对肾功能进展的关注。相反,肾功能恶化本身正是心血管风险的重要放大器。随着肾小球滤过率下降及白蛋白尿增加,容量负荷、尿毒症毒素蓄积及内环境紊乱等一系列改变,将持续加重心脏结构与功能损伤。因此,在临床决策中,应避免“重心血管、轻肾脏”或“单纯关注肾衰竭”的片面思维,而应坚持肾脏保护与心血管风险控制并重的“双通道干预”策略,这也是对Daniel Edmonston教授观点更为完整和深化的理解。
此外,CKD患者与CKM综合征人群在实际临床中呈现高度重合,这一点尤为值得关注。CKM综合征的提出,本质在于打破心血管、肾脏与代谢疾病之间的学科界限,而CKD恰恰位于这一交叉网络的核心节点。糖尿病、高血压、肥胖等代谢异常与CKD的发生发展密切相关,同时CKD本身亦可反过来加重心血管结构与功能异常。更为重要的是,一旦出现白蛋白尿升高或eGFR下降,即提示患者已进入CKM风险谱系。这意味着CKD不仅是一个终末器官损伤状态,更是系统性代谢紊乱与血管病变的重要标志。因此,从CKM视角重新审视CKD,有助于推动疾病管理由单一器官导向转向全身风险整合评估与干预。
在心血管风险构成方面,CKD患者“心血管事件谱转变”同样具有重要启示意义。随着CKD进展,虽然总体心血管事件发生率持续升高,但不同类型事件的构成发生显著变化。早期CKD患者的心血管事件以动脉粥样硬化性疾病为主,如冠心病及缺血性事件;而在中晚期CKD中,左心室肥厚、心力衰竭及肺动脉高压等非动脉粥样硬化性心血管事件的比例逐渐升高。这一现象提示,CKD相关心血管损伤具有明显的异质性,其病理基础并非单纯动脉粥样硬化的延续。其背后机制与CKD特有危险因素密切相关,包括尿毒症毒素、容量负荷过重、矿物质代谢紊乱以及贫血等,这些因素共同驱动心肌重构、血管钙化及心肺循环异常,形成典型的“肾源性心血管病”表型。因此,针对CKD患者的心血管管理,不能简单套用普通人群的防治模式,而需更加重视CKD患者非传统危险因素的识别与干预。
在治疗策略层面,当前指南推荐的延缓CKD进展四大类药物,即肾素-血管紧张素系统抑制剂(RASi)、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)、非甾体类盐皮质激素受体拮抗剂(nsMRA)以及胰高血糖素样肽-1受体激动剂(GLP-1RA),同样为CKD患者心血管事件及CKM综合管理提供了重要工具。这些药物虽作用机制各异,但均可同时作用于肾脏与心血管系统。此外,SGLT2抑制剂和GLP-1受体激动剂作为降糖药物,还可显著改善全身代谢状态。这一现象提示,这些药物的作用并非局限于CKM中的单一环节,而更可能通过多通路、多系统的协同调节,实现对CKM全周期的干预。换言之,这类药物并非传统意义上的“单器官靶向治疗”,而更接近于“系统性疾病调控策略”。
本次讲座的意义不仅在于强调CKD患者心血管风险高于肾衰竭风险这一关键认识,更在于引导临床医生在CKM综合征框架下重新理解CKD的本质。未来CKD管理应从单一终点控制转向多系统风险整合,从单靶点干预转向多通路协同调控,以期更有效改善患者的长期预后。
专家简介:
梁馨苓教授
广东省人民医院
医学博士、一级主任医师、教授、博士生导师
国家卫健委肾脏病透析质控专家委员会委员
中华医学会肾脏病学分会第十一届委员
中国医师协会肾脏内科医师分会常委
中关村肾脏病创新联盟CKM共管专委会主任委员、
广东省医学会肾脏病学分会副主任委员
广东省医院协会肾脏病防治与血液净化中心管理专委会主任委员
“百千万人才工程”国家级人选,获“有突出贡献中青年专家”荣誉称号、国务院政府特殊津贴专家、广东省医学领军人才;
主要研究领域为急性肾损伤、糖尿病肾病基础及临床研究。主持国家自然科学基金5项,发表SCI论文100余篇,获国家级专利4项,主编人卫专著《急性肾损伤》;主编人卫《内科学》思政案例库教材。




我要留言