编者按:
在血脂管理领域,低密度脂蛋白胆固醇(LDL-C)的长期管理理念更迭,脂蛋白(a)[Lp(a)]这一残余风险因素也已成为临床焦点。在第十五届中国胸痛中心大会(CCPCC15)上,中国医学科学院阜外医院李建军教授围绕LDL-C管理的革新方向、Lp(a)相关的关键证据及PCSK9抑制剂的临床价值3个维度,展开了精彩的报告。《心肾代谢时讯》现整理其精粹,为临床医生传递精准、前沿的防治策略。


一、新视野:LDL-C管理的深度探索与理念革新
1
双重挑战:年轻化趋势与达标困境
年轻人群血脂水平上升,动脉粥样硬化风险早期累积。美国一项针对20~39岁成人的连续横断面研究(n≈19.8M)显示,自2019年起,持续下降的总胆固醇(TC)和LDL-C趋势发生逆转,转为持续上升[1]。这一现象提示成年早期血脂恶化趋势显著,动脉粥样硬化风险可能在生命早期即开始累积加速,亟需加强对该人群的筛查与早期干预。
ASCVD患者LDL-C达标率严峻,无复发性事件患者成管理薄弱环节。美国cvMOBIUS-2注册研究纳入414 736例ASCVD患者,中位随访近2.5年,结果显示LDL-C自98 mg/dL降至83 mg/dL,但达标率极低:近70%患者未达到<70 mg/dL目标,高达87%患者未达到<55 mg/dL目标。尤为值得注意的是,无复发性ASCVD事件的患者,其LDL-C水平不降反升(β=+15.4 mg/dL),成为当前血脂管理中最易被忽视的薄弱环节[2]。
2
时间复利:早期大幅降低与长期累积获益
心肌梗死(MI)后早期LDL-C降幅≥50%显著改善长期预后。SWEDEHEART真实世界研究(n=49 966,首次MI,中位随访6.9年)证实,MI后6~10周实现LDL-C降幅≥50%,是降低长期风险与医疗负担的关键里程碑。与降幅<50%组相比,≥50%组患者复合主要不良心血管事件(MACE)风险降低23%,心血管死亡风险大幅降低46%,MI复发风险降低34%[3]。该研究为MI后早期强化降脂明确了具体的疗效目标(降幅≥50%),为药物选择提供了关键依据。
长期维持LDL-C低水平能带来随时间不断累积的额外心血管获益。CTT荟萃分析纳入13项他汀RCTs、99 360例受试者,进一步强调了降脂治疗的“时间复利”效应。分析显示,LDL-C每降低1 mmol/L,其心血管保护作用随着治疗时间的延长而显著增强。治疗1年时,MACE风险降低13%;而当治疗持续至第5年时,风险降低幅度增至22%(图1)[4]。这一发现深刻揭示了“持久降脂”的临床价值:长期维持LDL-C低水平能带来随时间不断累积的额外心血管获益。
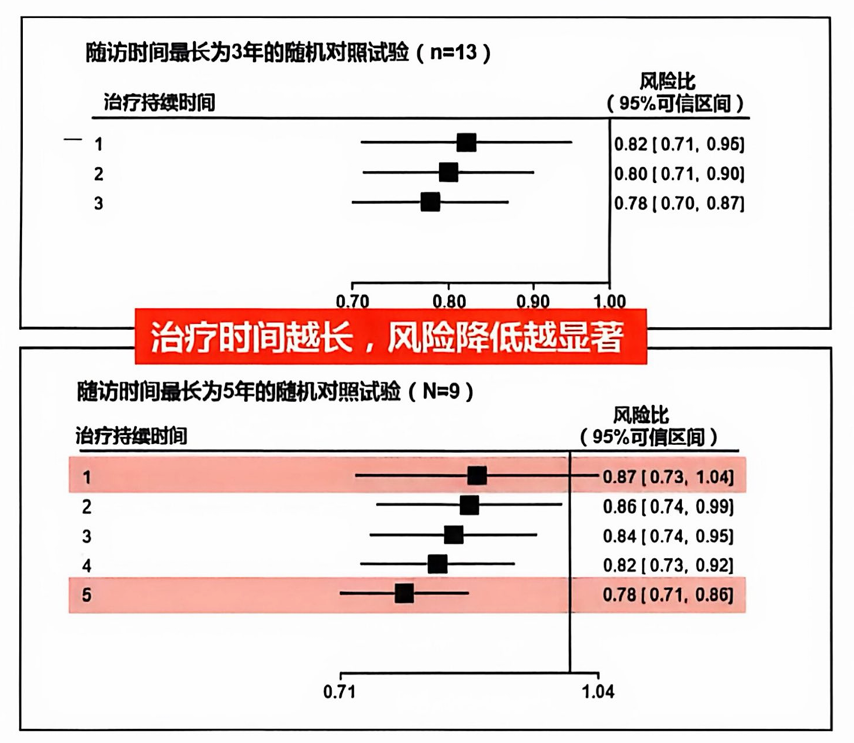
图1. 不同随访时长下,LDL-C降低1 mmol/L对MCE风险的影响
强化降脂安全性再确认,卒中后LDL-C<1.0 mmol/L安全可行。FOURIER研究的新分析发表于Circulation,结果显示对于既往有缺血性卒中史的患者,将LDL-C降至极低水平(<1.0 mmol/L,约40 mg/dL)不仅可大幅降低心血管事件复发风险,而且明确不增加脑出血风险[5]。这消除了临床对卒中患者强化降脂安全性的顾虑,支持了更积极的降脂目标。



二、新焦点:Lp(a)作为关键残余风险的证据涌现
1
Lp(a)独立预测易损斑块,优于传统风险标志物
一项基于AI定量冠脉CTA的影像学研究(n=547,无症状一级预防人群)发现,Lp(a)是识别易损斑块(低密度非钙化斑块-LDNCP)的独特、独立风险标志物。校正年龄、性别后,Lp(a)每升高1个标准差,与总斑块体积及各亚型体积增加均显著相关。在多变量模型中(校正LDL颗粒、hsCRP、冠脉钙化评分),仅Lp(a)与低密度非钙化斑块体积独立相关(β=0.45,P=0.013),而传统标志物(LDL-P、hsCRP)与任何斑块亚型均无显著关联[6]。这一研究提供了直接的影像学证据,表明Lp(a)升高特异性地促进形成高风险、易破裂的动脉粥样硬化斑块。
2
Lp(a)升高在人群中普遍存在,临床筛查严重不足
基于超3亿人数据库的全国性数据显示,尽管Lp(a)升高在人群中普遍存在(约20%),但其十年累计检测率仅0.2%。尽管检测量从2015到2024年增长了20倍,但年总检测比例仍低于0.3%[7]。
3
Lp(a)驱动斑块易损与支架内再狭窄
我国一项OCT影像学研究(n=146,伴支架内再狭窄的ACS患者)进一步揭示了Lp(a)在介入治疗预后中的不良影响。研究发现,Lp(a)升高(≥75 nmol/L)显著增加了易损斑块与新生动脉粥样硬化的风险。高Lp(a)组支架内新生动脉粥样硬化发生率高达91.2%,显著高于低Lp(a)组的50.9%;薄纤维帽斑块发生率也显著升高(38.2% vs 8.0%),巨噬细胞积聚率同样增加(82.4% vs 64.3%)。多因素分析证实,Lp(a)升高是支架内新生动脉粥样硬化和易损斑块的独立危险因素[8]。这表明Lp(a)不仅促进初始斑块的形成,还在支架内再狭窄的进程中扮演了关键角色。
4
Lp(a)水平与心血管风险及临床获益的量效关系
针对早发ASCVD患者(男<55岁,女<65岁)的研究发现,这一群体面临着Lp(a)升高的双重负担。早发患者比非早发患者平均年轻23.2岁,但Lp(a)升高的比例更高。结果显示,早发患者中Lp(a)≥50 mg/dL的比例为26.8%(非早发为24.3%),≥70 mg/dL的比例为18.8%(非早发为16.5%)[9]。无论是否早发,ASCVD事件风险均随Lp(a)水平升高而梯度增加。这些发现强调了Lp(a)在疾病早期发病中的重要作用,提示对高风险患者,尤其是早发ASCVD患者,进行Lp(a)检测具有极高的临床价值。
除了致病机制,降低Lp(a)能否带来临床获益也是关注焦点。一项基于三大队列真实世界数据的模型研究显示,Lp(a)降低幅度与复发性冠心病事件的减少呈正相关。对于Lp(a)≥200 nmol/L的人群,将Lp(a)降低150 nmol/L可多预防26%的事件/千人年,降低240 nmol/L可多预防84%的事件/千人年(相较于降低115 nmol/L的基线情况)[10]。
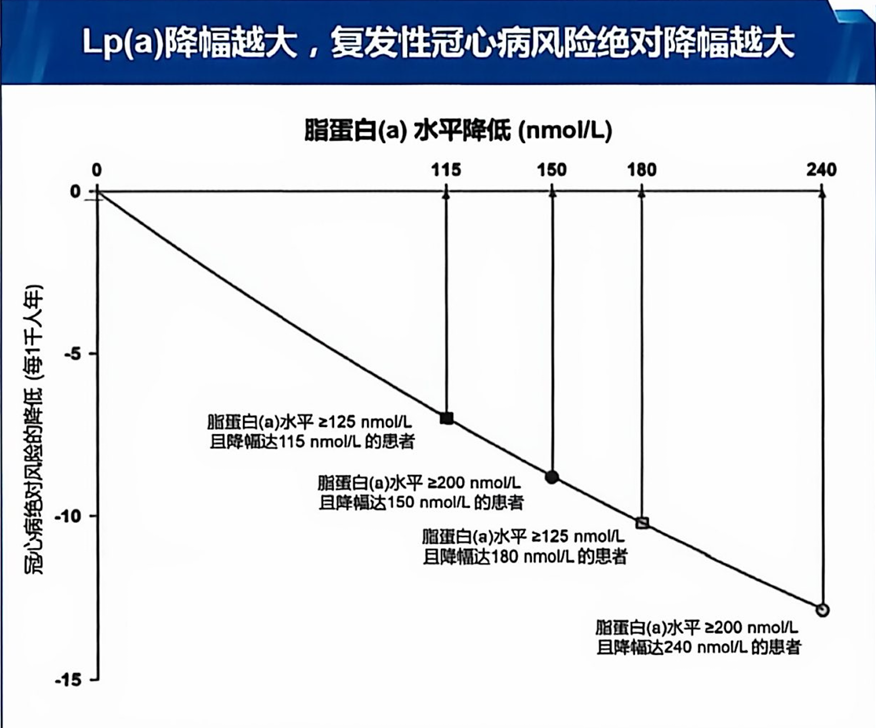
图2. Lp(a)降幅越大,复发性冠心病风险绝对降幅越大



三、新应答:PCSK9 抑制剂的“强效双效”价值兑现
当前,临床血脂管理面临着双重挑战:一是LDL-C管理需实现“早期大幅降低”与“长期持续维持”并重;二是Lp(a)作为关键残余风险因素,其筛查和干预势在必行。针对这两大挑战,单一的降脂手段往往难以兼顾。临床迫切需要一种能够同时满足“强效降LDL-C”与“显著降Lp(a)”的综合策略,以实现对心血管风险的全面管控。
在这一背景下,PCSK9抑制剂凭借其独特的作用机制,展现出了解决上述临床难题的潜力。作为一类强效降脂药物,PCSK9抑制剂不仅能显著降低LDL-C水平,还能在一定程度上降低Lp(a)水平,从而实现对多重风险因素的联合干预。以中国自主研发的PCSK9抑制剂托莱西单抗为例,临床研究数据显示,其最大LDL-C降幅近70%,能显著提高高危患者的达标率;Lp(a)方面最大降幅达47.6%,安全性较好,有利于保障患者长期治疗的依从性[11]。2025年发布的《全面管理血脂相关风险专家共识》也肯定了PCSK9单抗在降低Lp(a)方面的价值[12]。



结语
LDL-C管理理念已从单纯的“降脂”进化为“早期大幅降低并持久维持”,以最大化心血管获益;同时,Lp(a)作为被严重低估的残余风险因素,其致病证据日益充分,临床筛查与干预已刻不容缓。面对这两大核心挑战,PCSK9抑制剂凭借其“强效双效”的特性,为临床提供了理想的解决方案,为ASCVD患者带来更全面的心血管保护。



参考文献:
2.Satoshi Shoji, et al. Longitudinal LDL-C Control Among Patients With ASCVD and Elevated Baseline LDL-C: Insights From the cvMOBIUS-2 Registry. Presentation Number: Sa2113. Presented at AHA 2025.
3.Christian Reitan, et al. A 50% or Greater Reduction in LDL-Cholesterol Is Associated with Improved Long-Term Outcomes and Lower Health Care Utilization After Myocardial Infarction - a SWEDEHEART study. Presentation Number; Su2103- Presented at AHA 2025.
4.Federica Galimbert, et al. Cumulative exposure to low-density lipoprotein cholesterol levels explains the cardiovascular benefit over time in randomized clinical trials. Presentation-Number-MP492-Presented at AHA 2025.
5.Monguillon V, Kelly P, O'Donoghue ML, et al. Efficacy and Safety of Very Low Achieved LDL-Cholesterol in Patients with Prior Ischemic Stroke. Circulation. 2025 Nov 3.
6.Chen Gurevitz, et al. Lipoprotein(a) Selectively Associates with Vulnerable Coronary Plaque Phenotypes in Comparison with Other Established Risk Markers. Presentation Number: MP155. Presented at AHA 2025.
7.Mustafa Nagulb, et al. Increasing Rates of Lipoprotein(a) Testing in the United States from 2015-2024. An Analysis of 300 Million Individual Presentation-Number-Sa2114-Presented at AHA 2025.
8.Jiawen Chen, et al. Does Lipoprotein(a) Associate with In-Stent Neoatherosclerosis and Plaque Vulnerability Detected by Optical Coherence Tomography In Patients with Acute Coronary Syndrome? Abstract presented at AHA 2025.
9.Xingdi Hu, et al. Impact of Elevated Lipoprotein(a) on Cardiovascular Events in patients with premature ASCVD. A Nationally Representative Sample of US-Medicare-Medicaid-and-Commercial Enrollees—Presentation Number: MP2201. Presented at AHA 2025.
10.Christy L. Avery, et al. Estimated absolute coronary heart disease risk reduction with Lp(a) lowering among adults with atherosclerotic cardiovascular disease. Presentation Number: SA2107. Presented at AHA 2025.
11.Tafolecimab in Chinese Patients With Diabetes Mellitus. A Pooled Analysis of Efficacy and Safety Data From Phase 3 Randomized, Placebo-Controlled Trials
12.全面管理血脂相关心血管风险专家共识(2025)制订专家组,等. 中华心血管病杂志(网络版),2025,08(01):1-23.



我要留言