编者按:
巴特综合征(Bartter syndrome)是一种罕见的遗传性肾小管疾病,通常以严重低钾血症为典型特征。然而,近期Case Reports in Nephrology报道了一例颠覆传统认知的病例——一例39岁、巴特综合征Ⅳ型的女性患者,竟出现严重高钾血症(9.1 mmol/L)[1]!这一“矛盾性高钾血症”现象不仅挑战了临床对该病的固有认知,也警示我们需重新审视其电解质紊乱的复杂性。

积极参与讨论的幸运读者,
有机会获得
蔡广研教授主编新书
《慢性肾脏病全程管理新进展》 。

一反常态:
低钾疾病竟现高钾险情
巴特综合征是一种常染色体隐性遗传性盐重吸收障碍疾病,其特征为细胞外液容量减少、血压正常或降低,以及以低钾血症、低氯血症为主要表现的电解质异常,部分患者还会出现低镁血症。此外,患者常伴有高肾素、继发性醛固酮增多症及前列腺素E2水平升高,并表现为代谢性碱中毒。该疾病最常见于婴儿期,主要表现为生长发育迟缓。根据肾小管盐转运障碍的部位不同,巴特综合征可分为产前/新生儿型、经典型及Gitelman综合征等多种表型。
传统认知中,巴特综合征与严重低钾血症密切相关,而高钾血症的出现则被视为"矛盾性"现象。本文报告的这例患者为巴特综合征Ⅳ型,却表现出严重且难治的高钾血症,需多次血液透析干预。这一罕见病例不仅凸显了巴特综合征临床表现的多样性,也提示临床医生需对该疾病患者的电解质状态进行全面监测,并制定个体化的管理策略。深入研究此类病例的遗传变异及个体因素,对于完善巴特综合征的临床认知具有重要意义。
险象环生:
从常规补钾到高钾危象的紧急透析
患者女性,39岁,2岁时被诊断为巴特综合征Ⅳ型,同时患有纤维肌痛和失眠。患者依靠植入式输液港接受静脉补钾治疗,已维持7-8年。其家庭用药方案包括口服氯化钾溶液100 mmol每日三次,以及根据血钾水平每周一、三、五接受80~120 mmol静脉补钾(因无法耐受更高剂量口服氯化钾导致食管炎)。此外,患者还服用螺内酯100 mg/日和阿米洛利5 mg/日。
此次入院前,患者因多次呕吐和腹泻错过了预计的静脉补钾。入院时实验室检查显示血清钾升高至8.2 mmol/L,并伴有急性肾损伤(AKI),估算肾小球滤过率(eGFR)降至39 ml/min/1.73 m2(基线值为72 ml/min/1.73 m2)。其他实验室检查结果包括:动脉血气pH 7.351,二氧化碳分压(pCO2)40.1 mmHg,氧分压(pO2)90 mmHg,碳酸氢根(HCO3-)21.7 mmol/L;血清钠122 mmol/L;镁2.01 mg/dl;血糖84 mg/dl(4.7 mmol/L);氯98 mmol/L;血尿素氮17 mg/dl;血清肌酐1.69 mg/dl(基线1.12-1.23 mg/dl)。入院时心电图(EKG)显示QRS波增宽至138 ms,T波高尖,PR间期延长至195 ms(图1)。
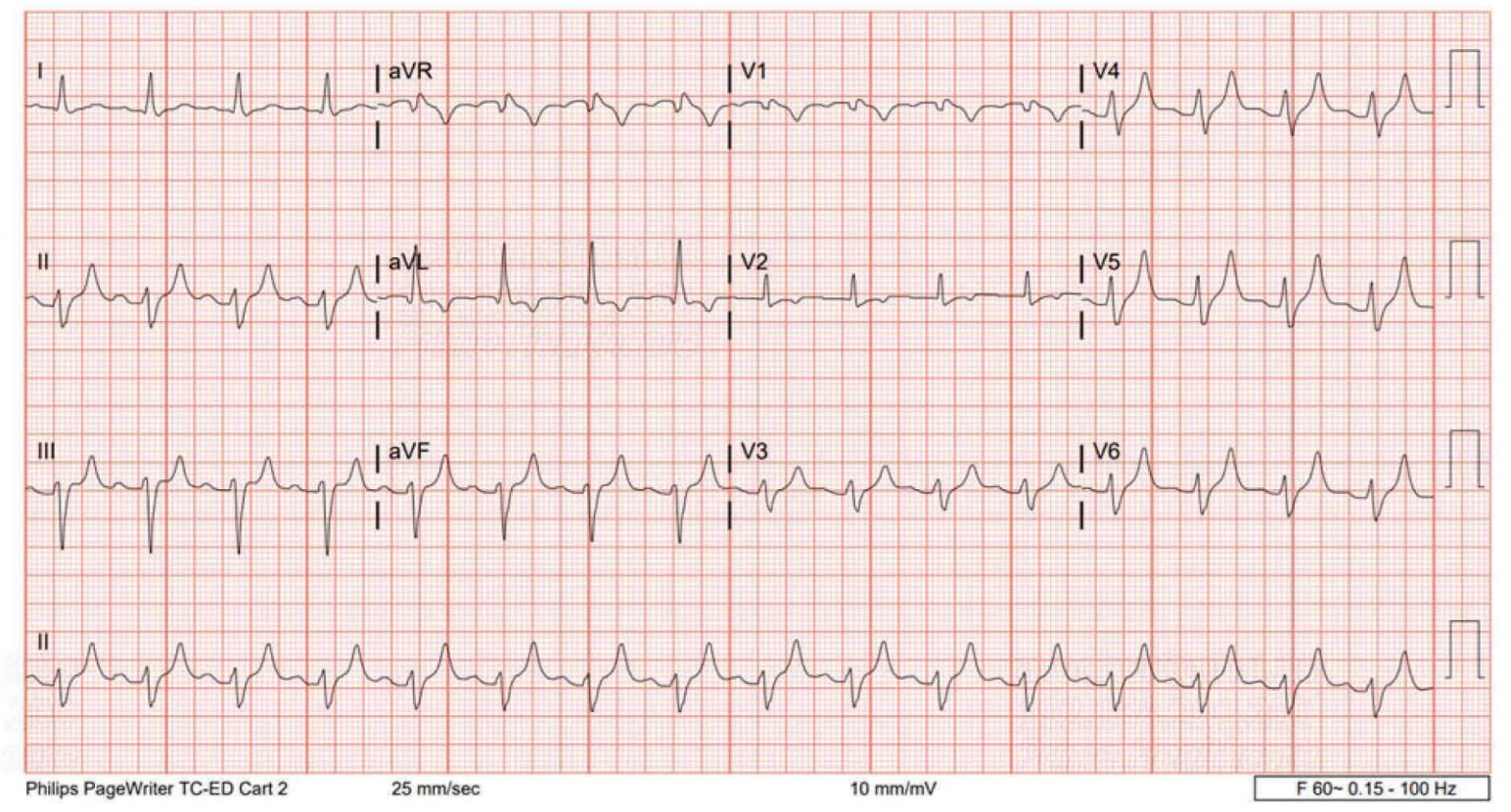
图1. 入院时心电图:示QRS波增宽、T波高尖及PR间期延长
入院后首先给予静脉注射1 g氯化钙,胰岛素10 IU+25 g 50%葡萄糖及环硅酸锆钠散 15 mg。复查EKG未显示高钾血症相关改变(图2),血清钾仍高达7.7 mmol/L,遂再次给予胰岛素和葡萄糖,血钾降至6.6 mmol/L后转入重症监护病房(ICU)。
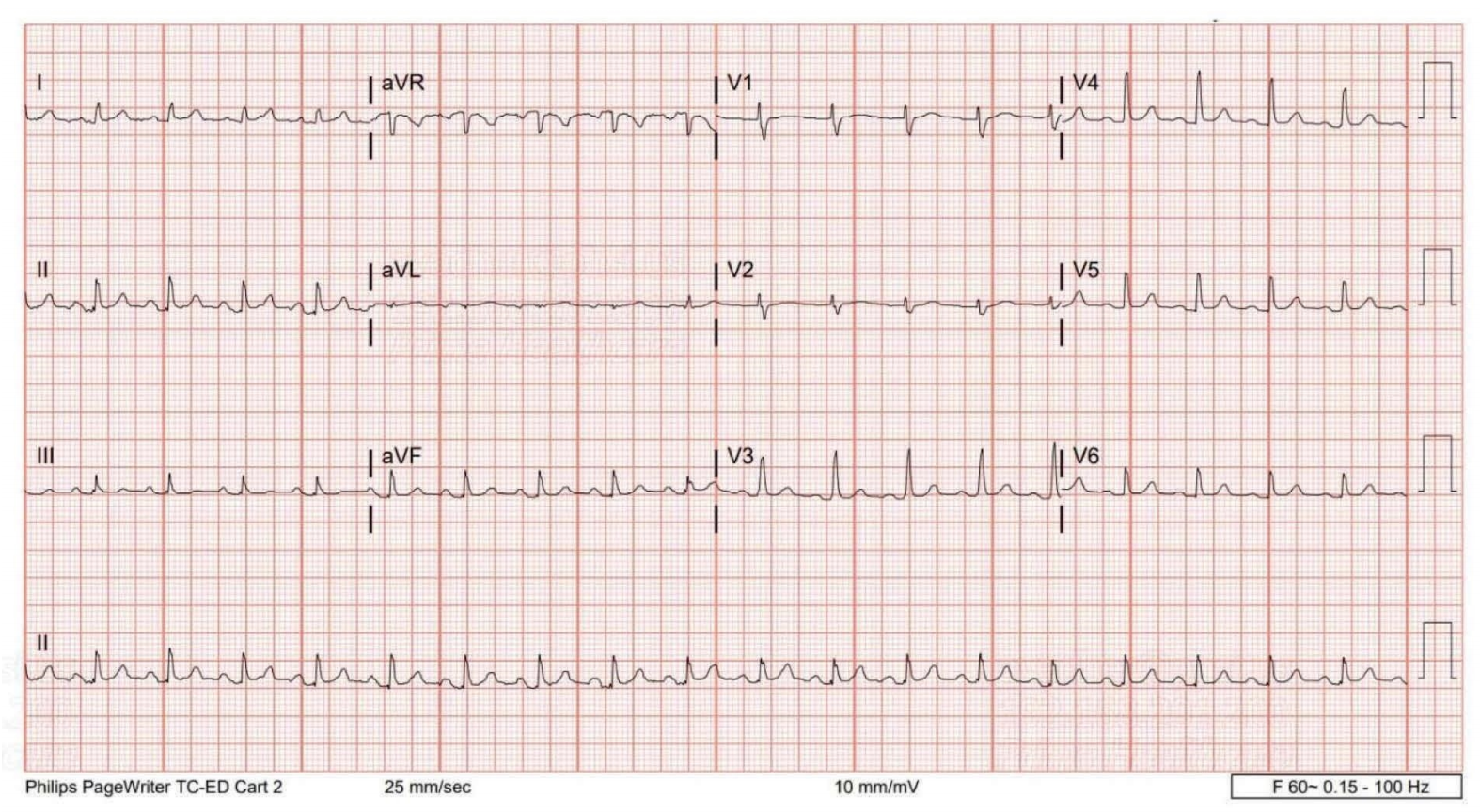
图2:复查心电图:T波高尖消失,PR间期及QTc恢复正常
转入ICU后6小时,患者血清钾再次升至9.1 mmol/L,心电图显示T波高尖、PR间期及QT间期延长。因高钾血症具有难治性,遂启动紧急血液透析治疗。首次透析持续2小时,透析液成分:钾1 mmol/L,钙1.25 mmol/L,碳酸氢盐35 mmol/L,钠138 mmol/L;透析器型号F160;血流量250 ml/min;透析液流量500 ml/min。透析后3小时血清钾降至7.0 mmol/L,但6小时后反弹至8.7 mmol/L。随后9小时内,患者共接受5 g静脉葡萄糖酸钙、100 mmol碳酸氢钠(随后持续碳酸氢钠输注)及额外10 g环硅酸锆钠散。
首次透析后12-18小时进行第二次透析,参数与首次相似(持续2小时,透析液钾1 mmol/L,血流量350 ml/min,透析液流量600 ml/min),透析后血钾降至6.0 mmol/L,但6小时后再次升至9.1 mmol/L。约9小时后进行第三次透析(持续2小时,透析液钾1 mmol/L,血流量350 ml/min,透析液流量800 ml/min),透析后血钾最终稳定至4.7 mmol/L。此后未再需要透析治疗,接下来48小时每12小时监测血钾均维持在正常范围。
深度解码:
“矛盾性高钾血症” 的机制探秘
01. 巴特综合征的分子病理与临床分型
巴特综合征是1962年首次报道的常染色体隐性罕见遗传病,发病率约1/1 000 000,核心病理为亨利袢升支粗段(TAL)离子通道功能缺失突变致肾小管盐耗损,进而引发球旁器增生、高肾素血症、正常血压性醛固酮增多症及低钾性代谢性碱中毒等一系列病理改变;其典型病症还包括显著低钾血症、低氯血症和高钙尿症,根源在于肾盐重吸收障碍[2,3]。
临床诊断通常依赖尿液电解质分析,表现为钠、钾、氯、钙及前列腺素E2水平升高。24小时尿钙排泄增加是巴特综合征与Gitelman综合征的重要鉴别点,后者尿钙排泄降低。血液检查常显示肾素和醛固酮水平升高,动脉血气分析提示代谢性碱中毒。基因检测可通过下一代测序靶向相关基因确诊。该疾病依突变基因不同分为五型,分别由SLC12A1、KCNJ1、CLCNKB、BSND及MAGED2基因突变导致,均以TAL段离子转运功能异常为核心,虽病症存在细微差异,但均会引发盐重吸收障碍及相关电解质紊乱,其中Ⅳ型还会伴随感音神经性耳聋。
02. 巴特综合征的临床特征与电解质紊乱
巴特综合征临床特征核心源于肾盐耗损与电解质紊乱,患者常表现为多尿、低渗尿引发的低血容量及脱水征象,如正常或低血压、头晕、乏力和多饮。早期症状包括喂养困难、出生后体重骤降、生长发育迟缓,且反复呕吐、腹泻、发热较常见。
低钾血症(血清钾<3.5 mmol/L)是最常见的电解质紊乱,可分为细胞内外钾分布异常(内部平衡紊乱)和钾摄入与排出异常(外部平衡紊乱)。通常,血清钾水平高于3.0 mmol/L时无明显症状。由于细胞内外钾离子浓度比对可兴奋组织的膜电位至关重要,低钾血症可导致肌肉无力或瘫痪、胃肠动力降低或肠梗阻,以及心律失常。低钾血症相关的心电图改变包括ST段压低、T波振幅降低和U波振幅增加。在Ⅰ型、Ⅲ型和Ⅴ型巴特综合征中,低钾血症是常见特征,而Ⅱ型巴特综合征在出生后最初几天可出现短暂性高钾血症(血清钾高于5.5 mmol/L)。低氯低钾性代谢性碱中毒和肾钙质沉着症也频繁出现。此外,低镁血症可导致手足搐搦,患者还可能出现特殊面容,如三角形脸、前额突出、大眼睛、招风耳和嘴角下垂。
03. 矛盾性高钾血症的机制探讨与管理
本病例中的成年巴特综合征患者表现出高钾血症,这与该疾病典型的低钾性代谢性碱中毒特征形成鲜明反差。巴特综合征因肾小管钾代谢异常,常常以低钾血症为核心表现,成年患者并发高钾血症的情况在临床中极为罕见。这一特殊表现不仅要求临床重新审视此类患者的电解质紊乱规律,更提示需结合影响肾小管功能的相关基因突变展开深入探究。
从病理生理机制来看,巴特综合征相关的高钾血症可能与钾稳态的短暂失衡有关,类似机制曾在Ⅱ型巴特综合征新生儿病例中被提及,但成年期发病的相关研究在现有文献中仍较为匮乏。结合本病例分析,患者入院前的频繁呕吐与腹泻引发低血容量,进而诱发肾前性急性肾损伤,这或是高钾血症的关键诱因。入院前2天患者血钾已升至6.0 mmol/L,且暂停补钾治疗的举措进一步加剧了电解质紊乱,急诊检查中122 mmol/L的血清钠水平也佐证了低血容量状态的存在。低血容量触发急性肾损伤后,远端小管与集合管的钾离子重吸收机制被激活,最终促成严重高钾血症的发生。
高钾血症(血清钾>5.0~5.5 mmol/L)的危害程度与血钾水平呈正相关,轻度升高时多无明显症状,血钾超过6.5 mmol/L则可能引发心律失常、肌肉无力甚至瘫痪等危及生命的表现。其致病机制在于细胞外钾浓度升高会削弱钠钾ATP酶泵维持的浓度梯度,降低心肌细胞静息膜电位,影响钠通道激活,进而导致心肌冲动传导延迟、去极化受阻,并呈现特征性心电图改变,且血钾升高速度对心电图的影响远超其绝对水平。临床中,高钾血症的诱因包括钾摄入过多、细胞内钾外流及肾脏排钾障碍,紧急处理需遵循停用钾源、钙剂稳定心肌细胞膜、促进钾向细胞内转移的原则,血液透析则是危及生命的高钾血症,尤其是药物治疗无效病例的首选方案。本病例患者经三次血液透析才控制高钾血症,也充分证实了血液透析在重症病例中的重要价值。

互动开始|病例讨论时间


怎么样?
这个病例是不是让人印象深刻?
欢迎您动动手指,参与互动
1.关于Bartter综合征患者出现高钾血症的可能机制,您认为下列哪项最符合该病例的临床推断,欢迎留言分享您的判断依据。(单选)
A.Bartter综合征本身导致肾脏钾排泄功能增强,造成高钾血症
B.患者因脱水引发肾前性急性肾损伤,导致钾排泄受限引发高钾血症
C.患者服用大量含钾药物过量所致的假性高钾血症
2.该Bartter综合征患者高钾血症治疗中,何种方式为最终控制血钾的关键手段?欢迎留言分享您的判断依据。(单选)
A.增加口服钾制剂及利尿剂调整
B.多次血液透析以快速降低难治性高钾
C.单纯使用胰岛素葡萄糖促细胞内钾转运
请选择您认为最合理的答案,并在APP评论区留下您的学术观点,与更多同行一起交流思考。



福利提示:
我们将从APP评论区中抽选2位积极参与讨论的幸运读者,赠送蔡广研教授 主编《慢性肾脏病全程管理新进展》一书。《慢性肾脏病全程管理新进展》涵盖了CKD全程管理总论、常见并发症管理、常见病因管理和特殊人群管理,力求系统展现患者教育、预防、诊断、治疗、康复等方面的国际新进展,并展示我国CKD领域的最新成果,旨在为该病全程管理提供务实可行的策略与范式。

结语
尽管高钾血症并非巴特综合征的典型特征,但其潜在发生风险强调了对此类患者进行全面监测和个体化管理的重要性。深入理解肾功能、药物作用和饮食因素之间的复杂相互作用,对于预防和有效管理这一特殊患者群体中的高钾血症至关重要。未来还需进一步研究巴特综合征中高钾血症的具体机制,特别是不同基因型与电解质紊乱表型的关联,以优化风险分层和治疗策略。
参考文献:
[1]Vadher A, et al. Paradoxical Hyperkalemia in Bartter Syndrome: A Case Report of Severe Resistant Hyperkalemia Requiring Hemodialysis. Case Rep Nephrol. 2025 Dec 11;2025:2644098.
[2]F. C. Bartter, P., et al. “Hyperplasia of the Juxtaglomerular Complex With Hyperaldosteronism and Hypokalemic Alkalosis,” Te American Journal of Medicine 33, no. 6 (1962): 811–828.
[3]D. Alla, et al., A Rare Presentation of Adult-Onset Bartter Syndrome: A Case Report, Cureus 15, no. 3 (2023): e36120.


我要留言