编者按:在急性冠脉综合征(ACS)的救治中,成功完成血运重建只是第一步。如何让脆弱的血管系统平稳度过事件后的“高危风暴期”,是决定患者长期预后的另一关键战场。长期以来,降脂治疗遵循着审慎的“逐步达标”原则,但这与ACS后早期极高的再发风险形成了鲜明的时间矛盾。
如今,随着强效降脂药物的涌现与临床证据的积累,一场深刻的治疗范式变革正在发生。核心降脂理念正从“阶梯调整”转向 “窗口期强化干预” ,强调在ACS发病后的黄金窗口内,快速地将低密度脂蛋白胆固醇(LDL-C)降至极低水平,以求最大程度地稳定斑块、降低再发风险。
在2025年“阜外血脂暨心血管代谢医学高峰论坛”上,海军军医大学第二附属医院(上海长征医院)梁春教授基于最新国际指南与前沿研究,对这一变革性策略进行了系统解读,深入阐述了其必要性、循证证据及临床实施路径,为ACS患者的全程优化管理提供了关键思路。

理念革新:
ACS事件后早期强化的必要性
急性冠脉综合征(ACS)事件如同一场心血管系统的地震,事件发生后,破裂的斑块和高度活跃的炎症使整个血管树处于极其脆弱的状态。循证医学揭示了一个严峻事实:ACS之后100天内,患者再发缺血事件的风险高达10%[1],这短短三个月堪称“最危险的时期”。
与此高风险窗口期形成尖锐矛盾的是传统降脂策略的滞后性。长期以来,临床实践遵循“阶梯治疗:模式:即从标准剂量他汀起始,4~12周后复查,若LDL-C未达标,再逐步考虑增加剂量或联用依折麦布。这缓慢的流程常导致患者在高风险时期无法有效地控制血脂水平,使患者持续暴露于再发的风险之中。
为破解这一时间困境,国际指南的导向已发生根本性转变。2025年欧洲心脏病学会(ESC)指南明确推荐:应在ACS住院期间即启动早期强化降脂治疗[1]。这一划时代的更新,旨在将治疗防线最大程度前移,其核心实践路径具体体现在以下两方面:
住院期间启动治疗
指南建议,对于入院前已接受降脂治疗但LDL-C未达标的患者,应在本次住院期间就强化治疗方案(I类推荐)。
对于初治患者,若预估单用他汀难以达标,应考虑在住院期间起始高强度他汀联合依折麦布的联合治疗(IIa类推荐)。
这彻底改变了以往出院后随访调整的惯例,将治疗起点提前到了临床医生最能掌控的住院阶段。
实践“更早、更低、更好”的原则
更早:干预时机从“数周后”提前至“数日内”,抓住急性期干预的黄金窗口。
更低:对ACS这类极高危患者,追求将LDL-C降至<1.4 mmol/L(约55 mg/dL)且较基线降低>50% 的严格双目标,体现了“越低越好”的原则。
更好:通过起始联合治疗,力求快速、深度降脂,以期在最短时间内稳定斑块、减轻炎症,从而为患者带来最大的近期与远期心血管获益。
因此,从“逐步达标”到“早期强化”的革新,本质上是一场与时间赛跑的风险管理策略升级。它要求临床医生像重视血运重建一样,重视急性期血脂的快速管控,从而在“百天高危期”内为患者建立起一道坚实的化学防御屏障。
证据支撑:
早期强化的有效性与安全性
早期强化降脂策略并非仅基于理论推演,而是建立在一系列严谨临床研究提供的坚实证据之上。这些证据围绕 “能否做到”“有何深层益处”以及“临床终点受益” 这三个核心问题,形成了完整的逻辑链条。
1.快速达标:从“可能”到“实现”
新策略的可行性首先被一系列药效学研究验证。EVOPACS、EVACS等研究证实了关键一点:在ACS入院早期(甚至在发病24小时内)启动高强度他汀、依折麦布与PCSK9抑制剂的三联或其他强化联合方案,能够在数日内实现LDL-C水平的断崖式下降。
具体数据显示,在心肌梗死后1天内联合他汀和PCSK9抑制剂,给药后24小时后即可观察到LDL-C的显著降低[2]。这使临床可迅速将患者的LDL-C水平降至<1.4 mmol/L(55 mg/dL),从而无缝衔接并覆盖了后续的“百天高危期”。这彻底解决了传统阶梯疗法的核心痛点,证明了新策略在技术上的高度可行性。
2.深层获益:超越数字的血管修复与抗炎
早期强化降脂的益处远不止于LDL-C的数字变化。得益于血管内影像学技术的进步,研究得以深入到斑块内部,观察治疗的直接效果。
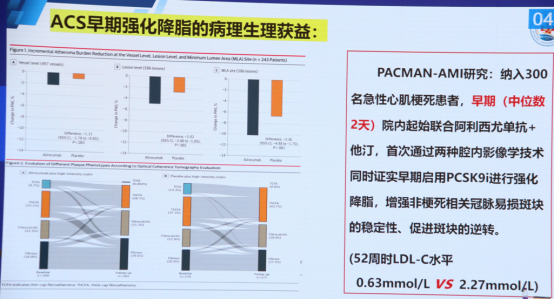
斑块逆转与稳定:PACMAN-AMI和HUVGENS等研究,通过血管内超声和光学相干断层扫描等技术发现,早期使用PCSK9抑制剂能够促进动脉粥样硬化斑块的体积减小(逆转),并显著增加保护性纤维帽的厚度[2]。这意味着,强化降脂治疗不仅清除了“坏胆固醇”,更直接加固了血管壁上最薄弱的环节,将不稳定的“活火山”转化为稳定的“休眠火山”。
抑制心肌炎症:动脉粥样硬化本质上是慢性炎症性疾病。EVACS研究的一项突破性子分析,首次通过PET-CT影像直观显示:ACS后早期使用依洛尤单抗,相比安慰剂,能更显著地减轻心肌局部的炎症反应[3]。这揭示了强化降脂在调脂之外的直接心脏抗炎保护作用,为改善患者预后开辟了另一条重要通路。
3.临床终点:初现曙光的硬结局获益
尽管最终结论有待大规模试验确认,但现有研究已在临床硬终点方面展现出积极的早期信号。
真实世界证据:一项意大利回顾性研究分析了500例急性心肌梗死患者,结果显示,采用早期强化并维持策略的患者,其出院后LDL-C达标率和长期主要不良心血管事件的发生率均显著优于传统阶梯治疗组[4]。
随机对照试验信号:一项纳入136例子极高危ACS患者的RCT显示,在PCI术后48小时内早期联用依洛尤单抗的治疗组,在90天内MACE(主要不良心血管事件)风险显著低于对照组,且安全性良好[5]。
以上这些证据层层递进,共同构建了强化降脂新策略的合理性:不仅能快速实现生化达标,更能带来稳定斑块、抗炎等多重病理生理获益,并已有趋势表明这些获益可转化为患者临床结局的改善。
实践启示与未来展望
基于当前坚实的药理学、影像学证据以及积极的早期临床信号,临床实践应果断拥抱这场理念变革。对于每一位ACS患者,尤其是高危和极高危者,管理策略应实现以下转变:
时机前移,视为急症处理:应将快速降脂视为与血运重建同等重要的急性期核心治疗之一,而非可延迟的门诊随访事项。
策略升级,起始即联合:摒弃“阶梯递增”的旧模式,对预估难以达标的患者,在住院期间即考虑起始高强度他汀联合依折麦布,必要时毫不犹豫地加用PCSK9抑制剂,力求在出院前或短期内将LDL-C击降至<1.4 mmol/L的深度目标。
目标多维,追求治本:治疗目标不应仅满足于LDL-C数值达标,更应致力于通过快速深度降脂来实现斑块稳定、炎症抑制等根本性的血管修复,从而为患者安然度过“百天高危期”并改善长期预后奠定坚实基础。
尽管现有证据已强力支持早期强化策略,但医学界仍在期待一个决定性的答案。为最终填补证据空白,一项备受瞩目的大规模随机对照试验——EVOLVE-MI研究正在进行中。该研究计划纳入4000名急性心肌梗死患者,其核心设计是无论患者基线血脂水平如何,均在发病后10天内启动PCSK9抑制剂(依洛尤单抗)治疗,并以心肌梗死、卒中、血运重建和全因死亡的复合终点作为主要评估指标,中位随访时间约3.5年[6]。这项研究的结果预计于2027年公布,其意义在于,它将首次在最高等级循证医学框架下,直接验证“在ACS极早期进行最强化降脂干预”能否转化为明确的硬终点获益,从而有望为这一策略的全面推广提供最终的定音之锤。
综上所述,从“逐步达标”到“早期强化”的演进,标志着ACS后血脂管理进入了一个全新的“窗口期管理”时代。它要求临床医生以更积极的姿态、更强的治疗组合,在疾病最关键的早期阶段为患者赢得最大的生存获益。这不仅是治疗工具的进步,更是“以患者风险为中心” 的现代医学思想,在临床决策中的深刻体现。
参考文献
1.Giugliano R P, et al. 2025 ESC Guidelines on the management of dyslipidemias: Key updates on early intensive lipid-lowering in ACS[J]. European Heart Journal, 2025.
2. Koskinas K C, et al. Effect of PCSK9 inhibition within 24 hours of acute myocardial infarction on LDL-C reduction: The EVOPACS study[J]. Journal of the American College of Cardiology, 2019, 73(16): 2059-2068
3.Zingg A, et al. Anti-inflammatory effects of early PCSK9 inhibition in acute coronary syndrome: Insights from FDG-PET imaging in the EVACS sub-study[J]. European Heart Journal - Cardiovascular Imaging, 2023, 24(Supplement_1): jead119.023.
4.Gragnano F, et al. Impact of a personalized, strike early and strong lipid-lowering approach vs conventional strategies on LDL-cholesterol levels and cardiovascular outcome in patients with acute myocardial infarction admitted across 3 different study periods[J]. Heart Journal - Cardiovascular Pharmacotherapy, 2025.
5.Wang Y, et al. Early addition of evolocumab to high-intensity statin and ezetimibe in extremely high-risk ACS patients undergoing PCI: a single-center randomized controlled trial[J]. Chinese Medical Journal, 2024, 137(5): 589-597.
6. Schwartz G G, et al. Design and rationale of the EVOLVE-MI trial: EVOLocumab Very Early after Myocardial Infarction[J]. American Heart Journal, 2023, 265: 1-10.


我要留言