编者按:
2025年12月19~21日,由中国医学科学院阜外医院心血管代谢中心、国家心血管病专家委员会心血管代谢医学专业委员会等多家权威机构联合举办的“2025阜外血脂暨心血管代谢医学高峰论坛”在京召开。本届论坛围绕高血脂及代谢性心血管疾病领域的前沿动态、临床实践与科研进展深入探讨,推动我国心血管疾病防控体系不断发展。在本次论坛上,“炎症与心血管残余风险”成为热点议题之一。
尽管心血管疾病治疗手段不断进步,越来越多患者血压、血脂、血糖等指标已得到良好控制,然而心梗、脑卒中等事件仍时有发生。为什么明明治好了却还会复发?这背后的隐形杀手究竟是什么?论坛期间,华中科技大学同济医学院附属协和医院心血管内科汪朝晖教授围绕着这些问题做了精彩演讲,解读了炎症在心血管残余风险中的关键作用及其临床应对策略。

炎症,心血管残余风险背后的“影子推手”
临床上常见的一个现象是:许多患者在接受了指南推荐的标准治疗后,即使其低密度脂蛋白胆固醇、血压、血糖等心血管危险因素已达标并已戒烟,仍然存在未来发生心梗、卒中等心血管事件的风险,这一现象被称为 “心血管残余风险”[1]。其背后反映的是,虽然传统治疗手段已得到广泛应用,但其预防心血管事件风险仍存在明显局限,亟需新的防控策略。
研究表明,慢性低度炎症是推动心血管残余风险的关键机制之一。这种炎症状态并非由感染引起,而是全身免疫系统长期、低度、持续的激活状态,如同“体内的慢火”,在血脂、血压控制良好的情况下,仍可持续驱动动脉粥样硬化进程,增加斑块不稳定性,最终导致心血管事件的发生[2~4]。
那么,如何评估这类炎症的风险?
目前临床最常用且证据最充分的生物标志物是高灵敏度C反应蛋白(hsCRP)[3]。多项研究显示,hsCRP水平升高与心血管事件风险呈线性相关。尤其值得关注的是,一项针对27 939例健康女性的前瞻性研究发现,在长达30年的随访期间,炎症所贡献的心血管事件风险甚至可能超过传统危险因素如LDL胆固醇,这凸显了炎症评估在心血管风险分层中的独立价值[3]。
除hsCRP外,其他炎症生物标志物如白介素-6(IL-6)、纤维蛋白原、血清淀粉样蛋白A等也具有一定预测价值,但在临床应用中,这些标志物尚未被证实优于hsCRP,且检测可及性通常较低。
在影像生物标志物方面,虽然用于检测血管炎症的影像学技术(如PET-CT、MRI)在研究领域前景看好,能够直观反映血管壁炎症活动及斑块稳定性,但这些影像生物标志物目前尚不被建议在常规临床环境中使用[2]。
抗炎治疗的“突破与困局”:从循证证据到临床应用
近年来,抗炎治疗在降低心血管事件风险方面的作用逐渐得到重视。多项具有里程碑意义的研究表明,抗炎治疗能够独立于传统的降压、降脂治疗,为心血管疾病患者带来额外的临床获益。然而,这一领域也存在一些争议和挑战,突显了治疗时机和人群选择的重要性。
他汀的抗炎价值
2008年发表的JUPITER研究是一项重要的临床试验,其结果显示,在hsCRP ≥2 mg/L、无高脂血症的健康人群中,使用瑞舒伐他汀治疗可显著降低主要心血管事件风险44% (图1)。该研究进一步显示,当患者同时实现血脂达标(LDL-C <70 mg/dl)和炎症控制(hs-CRP <1 mg/L)时,主要心血管事件风险降低79%[5]。
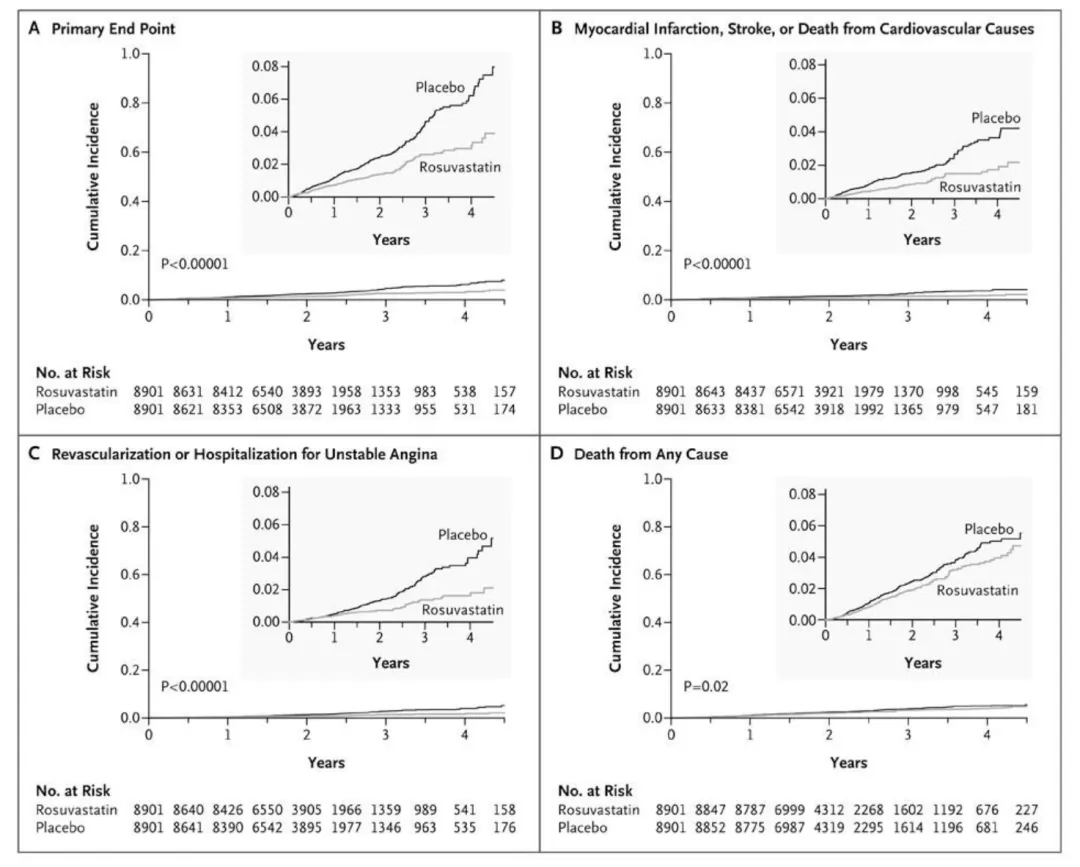
图1. 主要心血管事件
这表明,他汀类药物不仅具有降脂作用,还兼具抗炎效果,为心血管疾病的综合管理提供了新的方向。
靶向药物验证炎症学说
CANTOS研究是抗炎治疗领域的一个重要里程碑。该研究纳入10 061例既往有心肌梗死且hsCRP ≥2 mg/L的患者,随机接受卡那奴单抗(一种IL-1β单克隆抗体)或安慰剂治疗。结果显示,与安慰剂组相比,卡那奴单抗150 mg组的主要心血管不良事件(MACE)风险降低15%,且这一效果独立于血脂水平的变化[6]。该研究首次直接证实,抑制炎症本身即可降低心血管事件风险,进一步支持了炎症在动脉粥样硬化发展中的关键作用。
老药新用:秋水仙碱的争议与突破
秋水仙碱作为一种传统的抗炎药物,近年来在心血管疾病治疗中展现出新的应用前景。COLCOT研究纳入4745例近期心肌梗死患者,结果显示,在标准治疗基础上加用低剂量秋水仙碱(0.5 mg/d),可使主要心血管事件风险降低23%[7]。LODOCO-2研究进一步扩大适用人群,纳入5522例慢性冠心病患者,结果显示秋水仙碱治疗使主要心血管事件风险降低31%[8] (图2)。基于这些证据,多个国际指南已将其纳入推荐,用于特定人群的二级预防[9-12]。
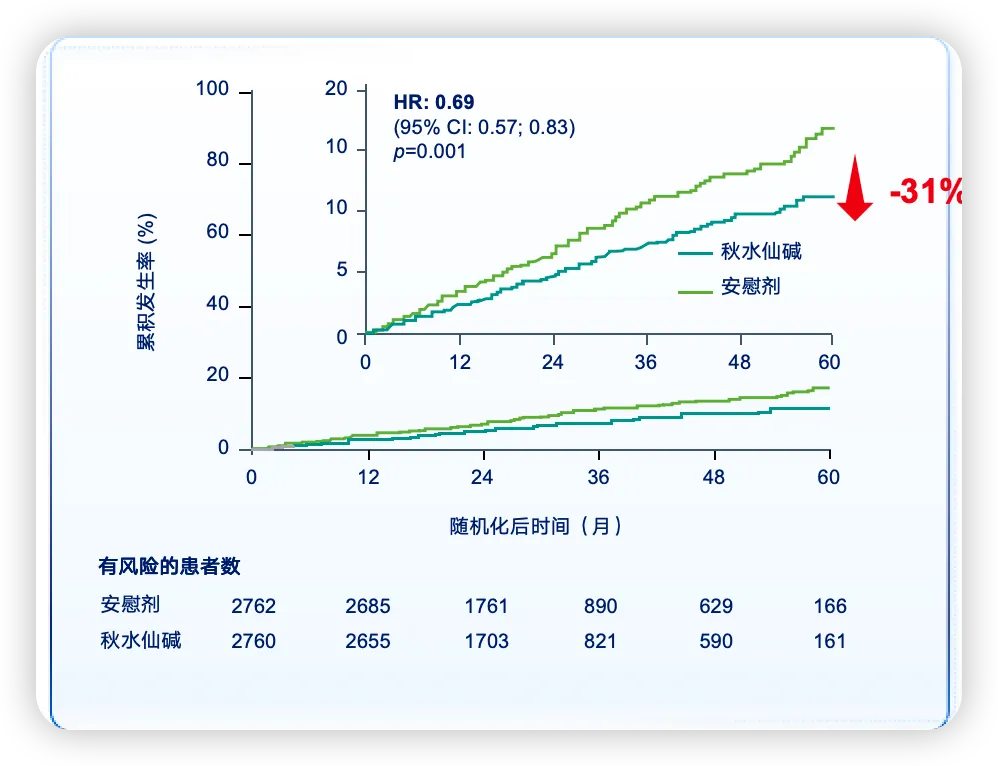
图2. 秋水仙碱/安慰剂的主要心血管事件累积发生率
然而,抗炎治疗并非适用于所有心血管疾病患者。CLEAR SYNERGY研究纳入7000余例接受PCI治疗的急性冠脉综合征患者,结果显示,在PCI术后72小时内开始使用秋水仙碱,尽管能显著降低CRP水平,但未能减少包括心血管死亡、心肌梗死、卒中在内的复合终点事件发生率[13]。这一结果提示,抗炎治疗的效果可能受到治疗时机和患者人群的影响,凸显了个体化治疗的重要性。
总之,抗炎治疗作为心血管疾病管理的新策略,已经从理论走向临床实践。然而,如何选择适宜的人群、确定最佳的治疗时机,以及平衡获益与风险,仍是临床医生面临的重要课题。未来,随着更多临床研究的开展,抗炎治疗有望在心血管疾病防治中发挥更加精准和有效的作用。
从筛查到干预:如何将炎症管理融入临床实践
2025 ACC共识及近年ESC指南均建议,将hsCRP作为心血管风险评估的常规项目,尤其在LDL-C控制良好但心血管事件仍复发的患者中[2]。其推荐的临床路径包括:
筛查先行:
建议将高灵敏度C反应蛋白(hsCRP)作为心血管风险评估的常规项目,并与低密度脂蛋白胆固醇(LDL-C)联合进行综合评估,以全面识别炎症相关的高危人群。
生活方式为基:
对所有hsCRP升高的患者,应优先推荐以地中海饮食为代表的抗炎饮食模式、规律运动及彻底戒烟,这些措施能有效降低系统性炎症水平。
药物干预有度:
在充分传统治疗基础上,对hsCRP持续升高且反复发生事件的患者,可考虑秋水仙碱等抗炎药物(Ⅱb类推荐)。
指南推广为盾:
需通过加强医生教育、完善临床路径、推动多学科协作,促进抗炎治疗策略在各级医疗机构的规范落地,从而真正降低心血管残余风险,改善患者长期预后。
未来展望
心血管疾病抗炎治疗的未来充满希望与潜力。
随着对炎症机制认识的不断深入,人们有望进一步优化现有抗炎药物的临床应用,包括更精准地界定适应人群、优化治疗时机与剂量,提升用药安全性与长期依从性。与此同时,针对新兴炎症靶点的药物研发正持续推进,例如靶向NLRP3炎性小体、CCR2通路、中性粒细胞胞外诱捕网等创新疗法,有望为患者提供更高效、更安全的抗炎选择。此外,抗炎治疗的应用范围也将从动脉粥样硬化性心血管疾病逐步拓展至心力衰竭、心肌炎、心房颤动等多种心血管疾病领域,形成更广泛的多模态干预体系。
未来,通过整合生活方式管理、传统药物治疗、靶向抗炎策略以及新型生物制剂,有望构建个体化、系统性的炎症管理方案,真正实现心血管残余风险的有效控制,推动心血管疾病防治迈向新阶段。
参考文献
1.Lawler PR, Bhatt DL, Godoy LC, et al. Targeting atherosclerosis in patients without obstructive coronary artery disease: a position statement from the ESC Working Group on Atherosclerosis and Vascular Biology. Eur Heart J. 2021;42(1):4-7.
2.Mensah GA, Bhatt DL, Bittner VA, et al. 2025 ACC expert consensus on the role of inflammation in cardiovascular disease risk assessment and management. J Am Coll Cardiol. 2025;S0735-1097(25)07555-2. [Epub ahead of print].
3.Ridker PM. A test in context: high-sensitivity C-reactive protein. J Am Coll Cardiol. 2018;72(25):3320-3333.
4.Libby P, B?ck M, Hansson GK. Inflammation in atherosclerosis: from mechanisms to therapeutic targeting. Immunity. 2025;58(10):2383-2401.
5.Ridker PM, Danielson E, Fonseca FA, et al. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med. 2008;359(21):2195-2207.
6.Ridker PM, Everett BM, Thuren T, et al. Antiinflammatory therapy with canakinumab for atherosclerotic disease. N Engl J Med. 2017;377(12):1119-1131.
7.Tardif JC, Kouz S, Waters DD, et al. Efficacy and safety of low-dose colchicine after myocardial infarction. N Engl J Med. 2019;381(26):2497-2505.
8.Nidorf SM, Fiolet ATL, Mosterd A, et al. Colchicine in patients with chronic coronary disease. N Engl J Med. 2020;383(19):1838-1847.
9.Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021;42(34):3227-3337.
10.Virani SS, Newby LK, Arnold SV, et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA guideline for the management of patients with chronic coronary disease. Circulation. 2023;148(9):e9-e119.
11.Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44(38):3720-3826.
12.Vrints C, Andreotti F, Koskinas KC, et al. 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J. 2024;45(36):3415-3537.
13.Jolly SS, Cairns JA, Yusuf S, et al. Colchicine early after PCI for acute coronary syndromes. N Engl J Med. 2025;392(7):633-642.

我要留言