编者按:心血管-肾脏-代谢综合征(CKM)作为一种新兴的临床概念,反映了肥胖、代谢紊乱、慢性肾病(CKD)和心血管疾病(CVD)之间的病理生理关联。美国心脏协会(AHA)发布的CKM分期为临床风险分层和个体化治疗提供了全新框架。本文基于American Journal of Medicine Open 2025年发表的病例研究,通过2个典型案例解析CKM早期识别与管理策略,强调早期干预对改善患者预后的重要性[1]。

有奖竞答
积极参与讨论的幸运读者,
有机会获得夏经钢教授、袁明霞教授主编的
《心血管-肾脏-代谢综合征防治手册》

CKM:
一场多器官联动的“慢性风暴”

CKM是指过量或功能异常的脂肪堆积、代谢紊乱、慢性肾病和心血管疾病之间相互作用而形成的临床综合征。随着全球肥胖和糖尿病患病率的上升,CKM健康问题已成为公共卫生领域的重大挑战。2023年AHA 首次提出CKM分期,通过整合PREVENT风险预测模型,实现对患者心血管疾病风险的分层,并根据不同分期制定靶向干预策略(图1)[2,3]。
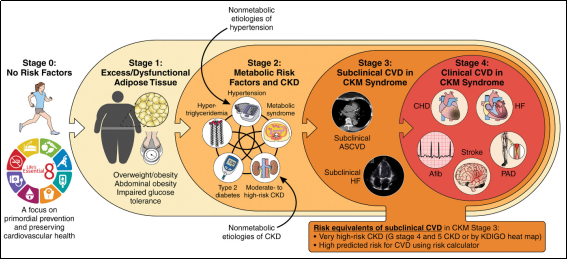
图1. CKM的临床分期
该框架的核心价值在于:将传统的单一疾病管理模式转变为多系统整合管理,通过早期识别CKM谱中的高危个体,以生活方式干预为基础,结合循证药物治疗,延缓疾病进展,甚至实现疾病阶段的逆转。
病例1:
体检报告里的“蛛丝马迹”

病例概述:看似无恙的中年女性
患者女性,57岁,因体检结果异常就诊。既往无明确慢性病病史,近3年尝试多种饮食(如生酮饮食、原始人饮食)减重未成功。每日遛狗45分钟,25年前已戒烟。母亲有糖尿病史,父亲有卒中史。患者诉每日睡眠8小时但日间疲劳,丈夫发现其打鼾。
体格检查:身高157.5 cm,体重75 kg,BMI 30.2 kg/m2,腰围84 cm,血压124/74 mmHg。实验室检查:空腹血糖(FBG)6.1 mmol/L(110 mg/dl),肌酐61.9 μmol/L(0.7 mg/dl)、估算肾小球滤过率(eGFR)103 ml/(min·1.73m2),糖化血红蛋白(HbA1c)5.5%,总胆固醇4.40 mmol/L(170 mg/dl),甘油三酯1.36 mmol/L(120 mg/dl),高密度脂蛋白胆固醇(HDL-C)1.34 mmol/L(52 mg/dl),低密度脂蛋白胆固醇(LDL-C)2.84 mmol/L(110 mg/dl)。
洞察先机:风险评估揭示的“远虑”
该患者被归类为CKM 1期,其特征为存在脂肪过度堆积(BMI 30.2 kg/m2)和中心性肥胖(女性腰围84 cm,接近88 cm的阈值),但无明显代谢异常或CKD。根据AHA推荐的生命要素筛查框架,患者存在以下潜在风险:空腹血糖轻度升高(6.1 mmol/L,提示糖耐量受损)、睡眠质量异常(打鼾、日间疲劳)及家族史阳性。
PREVENT风险评分显示:其10年总CVD风险为3%,动脉粥样硬化性心血管疾病(ASCVD)风险2%,心衰风险1%;30年总CVD风险达20%,ASCVD风险11%,心衰风险10%。PREVENT模型通过整合代谢、肾脏及社会因素,能精准地识别潜在的长期风险。
防微杜渐:生活方式的“精准导航”
CKM 1期患者的管理以生活方式干预为核心。建议每2~3年定期复查血压、血脂和血糖,对于空腹血糖升高者可适当增加监测频率。非评判性的减重咨询(如采用STOP-肥胖联盟工具包)可提高患者减重成功率。具体措施包括:饮食干预——推荐地中海饮食或DASH饮食,通过适度热量限制维持净能量负平衡;运动处方——每周至少150分钟中等强度或75分钟高强度有氧运动;体重管理——目标减重5%~10%。
针对患者的睡眠问题,建议进行多导睡眠图检查以排除阻塞性睡眠呼吸暂停,必要时给予持续气道正压通气治疗。此外,需评估社会决定因素(如收入、教育、社区资源)对健康的影响,通过社区卫生工作者或社工介入,消除潜在的治疗障碍。
病例2:
当代谢警报与肾脏预警交织

病例概述:被忽视的“三高”前奏
患者男性,60岁,白人,具有高血压、肥胖和糖尿病前期病史,多年未规律体检,未服用任何药物。无吸烟史。
体格检查:血压146/84 mmHg,心率88次/分,BMI 32 kg/m2,腰围105 cm。实验室检查:肌酐106.1 μmol/L(1.2 mg/dl),eGFR 68 ml/(min·1.73m2),FBG 7.6 mmol/L(136 mg/dl),HbA1c 7.9%,总胆固醇5.36 mmol/L(207 mg/dl),甘油三酯2.01 mmol/L(178 mg/dl),HDL-C 0.91 mmol/L(35 mg/dl),LDL-C 3.65 mmol/L(141 mg/dl),尿白蛋白/肌酐比值(UACR)45 mg/g(正常<30 mg/g)。
靶向聚焦:风险评估锁定的核心风险
患者符合CKM 2期诊断标准:存在代谢综合征(腹型肥胖、高甘油三酯、低HDL-C、高血压、糖尿病)和中风险CKD[eGFR 60~89 ml/(min·1.73m2),UACR 30~300 mg/g,KDIGO G2A2期]。PREVENT评分显示其10年总CVD风险20%,ASCVD风险13%,心衰风险11%。值得注意的是,PREVENT模型通过纳入CKD和肥胖参数,准确地捕捉了患者的整体风险,其总CVD风险≥20%提示需启动强化干预。此外,单次UACR升高需再次检测确认,以排除生理性波动。
合力施治:多靶点药物的“协同作战”
CKM 2期的治疗目标是控制代谢风险因素、保护肾功能、预防CVD进展。
1. 多学科协作:通过跨学科团队(心内科、肾内科、内分泌科)协作,优化药物滴定和依从性管理,并定期评估社会决定因素对治疗的影响。
2. 风险因素控制:血糖目标HbA1c<7%,血压目标<130/80 mmHg,LDL-C需降低30%~50%。他汀类药物选择中-高强度方案;降压治疗优先使用肾素-血管紧张素-醛固酮系统(RAAS)抑制剂,如血管紧张素Ⅱ受体拮抗剂(ARB),以减少蛋白尿并保护肾功能。
3. 降糖治疗:钠-葡萄糖协同转运蛋白2抑制剂(SGLT-2i)抑制剂被优先推荐,因其可延缓CKD进展、降低心衰和心血管死亡风险。胰高糖素样肽-1受体激动剂(GLP-1RA)也可考虑,FLOW试验证实其能同时改善肥胖、糖尿病及心肾结局。对于HbA1c≥7.5%者(如本例7.9%),可联合二甲双胍(500 mg起始,逐渐加量至1000 mg bid)以增强血糖控制,尤其在GLP-1RA费用受限的情况下。
现有证据显示,两者联合可产生协同效应,尤其适用于CKM风险高的患者(如本例总CVD风险20%)。KDIGO 2024指南支持这种联合策略,尽管随机对照试验数据尚在积累中。Meta分析提示,联合用药可能增加胃肠道反应和注射部位反应,但未增加严重不良事件风险。临床决策需结合患者风险特征(如SGLT-2i更适用于心衰/CKD,GLP-1RA更适用于肥胖)、药物可及性及患者偏好。
提问时间到:
欢迎大家下载《心肾代谢时讯》APP, 并在APP评论区留下您的学术观点,与更多同行一起交流思考。 扫码 结语 CKM 1~2期是疾病干预的关键窗口。通过PREVENT风险评分精准识别高危个体,以生活方式干预为基础,结合SGLT-2i、GLP-1RA等新型药物,可有效延缓疾病进展。临床实践中需重视多系统风险的整合评估,避免单一指标的局限性。下一篇将聚焦CKM 3~4期的复杂病例管理,探讨亚临床动脉粥样硬化和临床CVD的综合治疗策略。 参考文献: 1. Javaid A, et al. Am J Med Open. 2025;13:100089. 2.Ndumele CE, et al. Circulation 2023;148(20):1606–1635. 3. Khan SS, et al. Circulation 2023;148(24):1982–2004. 声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。


二维码即可下载


我要留言